题目内容
在KI淀粉溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝,这是因为 .其离子方程式是 .在上述蓝色溶液中滴加足量Na2SO3溶液,蓝色逐渐消失,这是因为(用离子方程式表示) .以上实验条件下,ClO-、I2、SO42-的氧化性由强到弱的顺序是 .
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:溶液立即变蓝,说明生成碘,NaClO在酸性条件下氧化KI生成碘,滴加足量Na2SO3溶液,蓝色逐渐消失,说明碘与Na2SO3发生氧化还原反应,以此解答.
解答:
解:在KI淀粉溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝,说明生成碘,NaClO在酸性条件下氧化KI生成碘,反应的离子方程式为2I-+ClO-+2H+═I2+Cl-+H2O,氧化性:ClO->I2,在上述蓝色溶液中滴加足量Na2SO3溶液,蓝色逐渐消失,说明碘与Na2SO3发生氧化还原反应,反应的离子方程式为SO32-+I2+H2O═SO42-+2H++2I-,可说明氧化性I2>SO42-,则氧化性ClO->I2>SO42-,
故答案为:I-能被HClO氧化成I2,I2遇淀粉变蓝;2I-+ClO-+2H+═I2+Cl-+H2O;SO32-+I2+H2O═SO42-+2H++2I-;ClO->I2>SO42-.
故答案为:I-能被HClO氧化成I2,I2遇淀粉变蓝;2I-+ClO-+2H+═I2+Cl-+H2O;SO32-+I2+H2O═SO42-+2H++2I-;ClO->I2>SO42-.
点评:本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力的考查,注意把握物质的性质以及氧化性、还原性的比较角度,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
对于反应4A+B=2C,下列说法正确的是( )
| A、某温度下,化学反应速率无论是用A、B、C何种物质来表示,其化学反应速率的数值相同 |
| B、在其他条件不变的情况下,降低温度,一般化学反应速率降低 |
| C、在其他条件不变的情况下,增大压强,单位体积内活化分子百分数一定增大,化学反应速率一定增大 |
| D、若增大或减少A物质的量,化学反应速率一定会发生明显的变化 |
将两粒相同大小的钠,一粒用铝箔包好为甲,另一粒为乙,将甲、乙两粒钠分别投入足量的水中,收集所得气体,气体的体积大小关系是( )
| A、乙多 | B、甲多 |
| C、一样多 | D、无法确定 |
下列物质属于有机物的是( )
| A、氰化钾 KCN |
| B、氰酸铵 NH4CNO |
| C、聚乙炔 (C2H2)n |
| D、碳化硅 SiC |
将一定量的甲烷完全燃烧,使所生成的气体依次通过装有足量无水CaCl2和NaOH的玻璃管.结果盛NaOH的玻璃管质量增加了1.1g,则原来甲烷在标准状况下的体积为( )
| A、2.24L |
| B、1.12L |
| C、0.56L |
| D、0.28L |

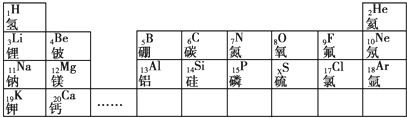
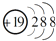 表示的是(写粒子符号)
表示的是(写粒子符号)