题目内容
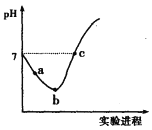
【题目】常温下,向20mL某浓度的硫酸溶液中滴入0.1molL-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图,下列分析正确的是( )
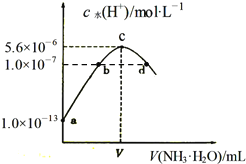
A.V=40
B.c点所示溶液中:c(H+)-c(OH-)=2c(NH3H2O)
C.d点所示溶液中:c(NH4+)=2c(SO42-)
D.NH3H2O的电离常数K=10-4molL-1
【答案】C
【解析】
根据加酸加碱抑制水的电离,加盐促进水的电离规律分析本题。
未加氨水时硫酸溶液中水电离出的![]() ,则硫酸溶液中
,则硫酸溶液中![]() ,硫酸的浓度是
,硫酸的浓度是![]() ,
,
A. c点水电离程度最大,此时铵根离子浓度最大,对水的电离促进程度最大,所以两者恰好完全反应生成硫酸铵,而稀硫酸的浓度为![]() ,硫酸溶液中氢离子的浓度为
,硫酸溶液中氢离子的浓度为![]() ,氨水的浓度是
,氨水的浓度是![]() ,所以氨水的体积也是20mL,即
,所以氨水的体积也是20mL,即![]() ,故A错误;
,故A错误;
B. c点所示溶液是硫酸铵溶液,溶液中质子守恒:![]() ,所以溶液中存在:
,所以溶液中存在:![]() ,故B错误;
,故B错误;
C. d点溶液中的溶质是和(NH4)2SO4和NH3·H2O,溶液呈中性,根据电荷守恒:![]() ,而,
,而,![]() ,所以
,所以![]() ,故C正确;
,故C正确;
D. c点溶液中水电离出的![]() ,该溶液中
,该溶液中![]() ,
,![]() ,
,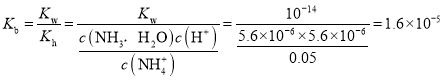 ,
,
故D错误;
答案:C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目