题目内容
(12分)为探究如何尽可能多的使NO2被水吸收,某活动小组设计并完成了以下实验。
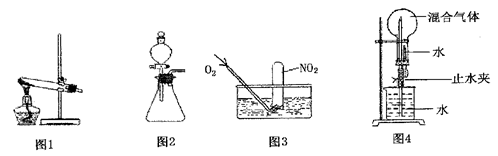
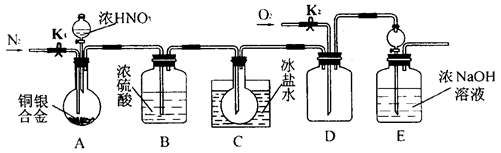
(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
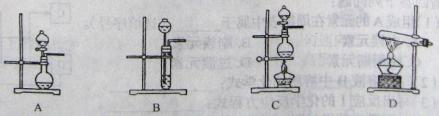
①根据反应原理他们选用了相同的装置 (填“图l”或“图2”)分别制取NO2和O2。
②写出铜与浓硝酸反应的离子方程式 。
③写出过氧化氢溶液与MnO2制取O2时的化学方程式 。
④收集NO2的方法是 。
(2)活动小组的同学做了如下准备工作:用气囊收集好纯净的O2,收集了一试管NO2,用干燥的烧瓶收集了一定比例的NO2和O2的混合气体。
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是:
。
②利用图4吸收气体时,其操作和现象为:
。
③若图4中混合气体NO2和O2全部被吸收时所得溶液物质的量浓度为 mol/L(保留两位有效数字)。

(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
①根据反应原理他们选用了相同的装置 (填“图l”或“图2”)分别制取NO2和O2。
②写出铜与浓硝酸反应的离子方程式 。
③写出过氧化氢溶液与MnO2制取O2时的化学方程式 。
④收集NO2的方法是 。
(2)活动小组的同学做了如下准备工作:用气囊收集好纯净的O2,收集了一试管NO2,用干燥的烧瓶收集了一定比例的NO2和O2的混合气体。
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是:
。
②利用图4吸收气体时,其操作和现象为:
。
③若图4中混合气体NO2和O2全部被吸收时所得溶液物质的量浓度为 mol/L(保留两位有效数字)。
(12分)
(1)①图2(1分)
②Cu+4H++2NO3-=Cu2++2NO2↑+2H2O(2分)
③2H2O2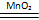 2H2O+O2↑(2分)
2H2O+O2↑(2分)
④瓶口向上排空气法(1分)
(2)①有利于控制氧气气流的速度(控制氧气的量)(2分)
②将胶头滴管中的水挤压进烧瓶,然后打开止水夹,可以看到烧杯中的水进入烧瓶形成喷泉(2分)
③0.036(2分)
(1)①图2(1分)
②Cu+4H++2NO3-=Cu2++2NO2↑+2H2O(2分)
③2H2O2
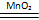 2H2O+O2↑(2分)
2H2O+O2↑(2分)④瓶口向上排空气法(1分)
(2)①有利于控制氧气气流的速度(控制氧气的量)(2分)
②将胶头滴管中的水挤压进烧瓶,然后打开止水夹,可以看到烧杯中的水进入烧瓶形成喷泉(2分)
③0.036(2分)
考查氮的氧化物的性质
(1)①两反应过程均为固液不加热,故一般选用图2作为气体的发生装置;
②Cu+4H++2NO3-=Cu2++2NO2↑+2H2O(2分)
③MnO2起催化作用:2H2O2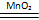 2H2O+O2↑(2分)
2H2O+O2↑(2分)
④NO2密度大于空气且可与水反应,故一般采用向上排空气法收集(1分)
(2)①直接制取O2气体,更有利于控制气体的用量及比例,更好的切合实验目的
②这是一套喷泉实验装置,挤压胶头滴管内的水,内部气压减小,打开止水夹,烧杯中的水即可进入烧瓶
③气体全部被吸收时,发生反应为:4NO2+O2+2H2O=4HNO3,设烧瓶的容积为VL
硝酸的物质的量为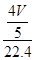 mol,所得硝酸溶液的浓度为
mol,所得硝酸溶液的浓度为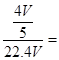 0.036mol/L
0.036mol/L
(1)①两反应过程均为固液不加热,故一般选用图2作为气体的发生装置;
②Cu+4H++2NO3-=Cu2++2NO2↑+2H2O(2分)
③MnO2起催化作用:2H2O2
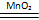 2H2O+O2↑(2分)
2H2O+O2↑(2分)④NO2密度大于空气且可与水反应,故一般采用向上排空气法收集(1分)
(2)①直接制取O2气体,更有利于控制气体的用量及比例,更好的切合实验目的
②这是一套喷泉实验装置,挤压胶头滴管内的水,内部气压减小,打开止水夹,烧杯中的水即可进入烧瓶
③气体全部被吸收时,发生反应为:4NO2+O2+2H2O=4HNO3,设烧瓶的容积为VL
硝酸的物质的量为
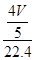 mol,所得硝酸溶液的浓度为
mol,所得硝酸溶液的浓度为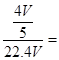 0.036mol/L
0.036mol/L
练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
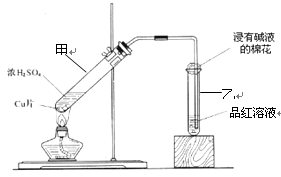
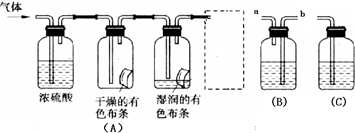
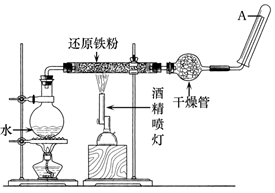
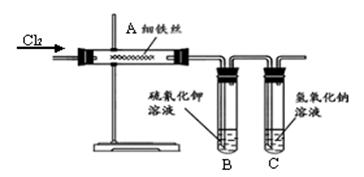
 试管B中的现象是___________________,
试管B中的现象是___________________,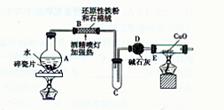
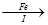 FeSO4溶液
FeSO4溶液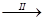 FeSO4·7H2O晶体
FeSO4·7H2O晶体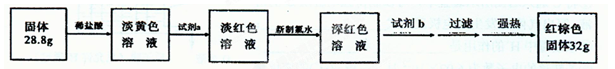
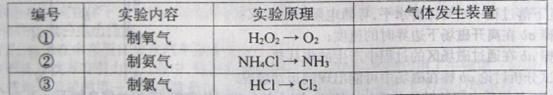
 的
的 装置制备O
装置制备O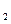 ,则选择的试剂为 (填化学式);若用上述制备O
,则选择的试剂为 (填化学式);若用上述制备O 进行,写出反应④的离子方程式。 。
进行,写出反应④的离子方程式。 。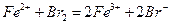 ,现向100mL的
,现向100mL的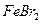 溶液中通入标准状况下Cl
溶液中通入标准状况下Cl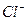 与
与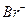 的物质的量浓度相等(设通入Cl
的物质的量浓度相等(设通入Cl