题目内容
下表是实验室制备气体的有关内容:
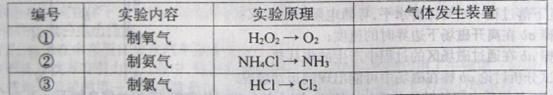
(1)上述气体中,从制备过程看,必须选择合适的氧化剂才能实现的是 (填气体的化学式);从反应原理看,明显不同于其它两种气体的是 (填气体的化学式);从收集方法来看,只能用一种方法收集的是 (填气体的化学式)。
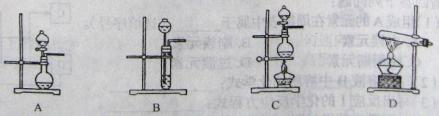
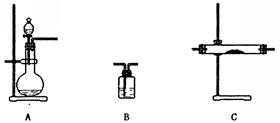
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其选项填入表中相应编号的空格中。
(3)若用上述制备NH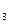 的
的 装置制备O
装置制备O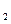 ,则选择的试剂为 (填化学式);若用上述制备O
,则选择的试剂为 (填化学式);若用上述制备O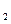 的装置制备NH
的装置制备NH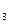 ,则选择的试剂的名称为 。
,则选择的试剂的名称为 。
(4)若用排空气法收集Cl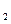 ,请画出气体收集装置图 。
,请画出气体收集装置图 。
(5)有下列无机物的转化关系,已知B和Y是上述三种气体中的两种。
a.当w为MnO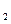 时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式 。
时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式 。
b.当w为KMnO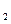 时,反应①加热才能进行,反应④不加热就能
时,反应①加热才能进行,反应④不加热就能 进行,写出反应④的离子方程式。 。
进行,写出反应④的离子方程式。 。
(6)已知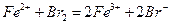 ,现向100mL的
,现向100mL的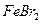 溶液中通入标准状况下Cl
溶液中通入标准状况下Cl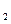 3.36L,充分反应后,测得溶液中
3.36L,充分反应后,测得溶液中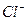 与
与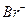 的物质的量浓度相等(设通入Cl
的物质的量浓度相等(设通入Cl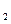 前后溶液体积不变),则原
前后溶液体积不变),则原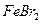 溶液中溶质的物质的量浓度为 。
溶液中溶质的物质的量浓度为 。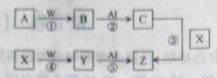

(1)上述气体中,从制备过程看,必须选择合适的氧化剂才能实现的是 (填气体的化学式);从反应原理看,明显不同于其它两种气体的是 (填气体的化学式);从收集方法来看,只能用一种方法收集的是 (填气体的化学式)。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其选项填入表中相应编号的空格中。

(3)若用上述制备NH
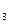 的
的 装置制备O
装置制备O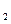 ,则选择的试剂为 (填化学式);若用上述制备O
,则选择的试剂为 (填化学式);若用上述制备O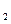 的装置制备NH
的装置制备NH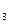 ,则选择的试剂的名称为 。
,则选择的试剂的名称为 。(4)若用排空气法收集Cl
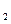 ,请画出气体收集装置图 。
,请画出气体收集装置图 。(5)有下列无机物的转化关系,已知B和Y是上述三种气体中的两种。
a.当w为MnO
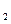 时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式 。
时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式 。b.当w为KMnO
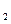 时,反应①加热才能进行,反应④不加热就能
时,反应①加热才能进行,反应④不加热就能 进行,写出反应④的离子方程式。 。
进行,写出反应④的离子方程式。 。(6)已知
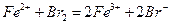 ,现向100mL的
,现向100mL的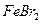 溶液中通入标准状况下Cl
溶液中通入标准状况下Cl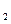 3.36L,充分反应后,测得溶液中
3.36L,充分反应后,测得溶液中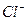 与
与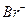 的物质的量浓度相等(设通入Cl
的物质的量浓度相等(设通入Cl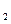 前后溶液体积不变),则原
前后溶液体积不变),则原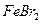 溶液中溶质的物质的量浓度为 。
溶液中溶质的物质的量浓度为 。

略

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
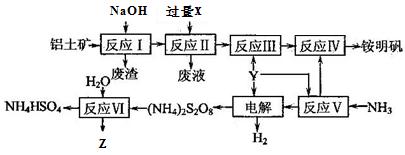
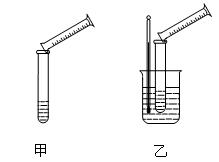
 生反应,设计并完成了如图所示
生反应,设计并完成了如图所示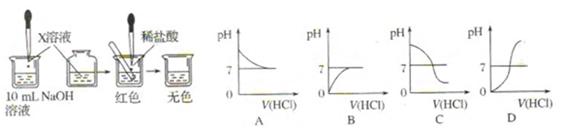
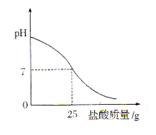
 试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。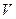 )/mL
)/mL 度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。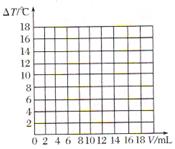
 (Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。 O
(Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。 O 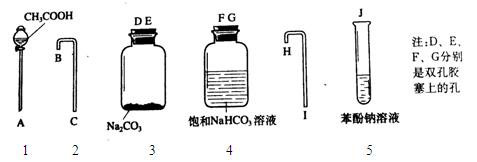
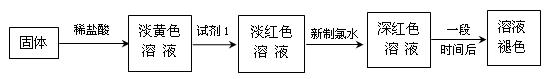
 2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤。
步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤。