题目内容
12.用下列实验装置进行的实验,能达到相应的实验目的是( )| A. | 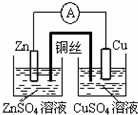 铜锌原电池 | B. | 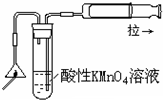 检验火柴头燃烧产生的SO2 | ||
| C. |  分液操作 | D. | 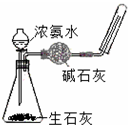 制取氨气 |
分析 A.离子不能向两极定向移动;
B.进气管太短,没有插入到液面以下;
C.分液漏斗下端应紧贴烧杯内壁;
D.氨气易挥发,碱石灰具有吸水作用.
解答 解:A.没有形成闭合回路,离子不能向两极定向移动,不能形成原电池,故A错误;
B.进气管太短,应将进气管插入到液面以下,故B错误;
C.分液漏斗下端应紧贴烧杯内壁,防止液体飞溅,故C错误;
D.水与生石灰反应放热,促进氨气挥发,碱石灰具有吸水作用,氨气密度比水小,可用向下排空法收集,故D正确.
故选D.
点评 本题综合考查化学基本操作,涉及原电池、物质的检验、分离以及制备等操作,侧重于学生化学设计和评价的能力的考查,为高考常见提醒,难度不大.

练习册系列答案
相关题目
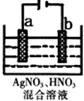
3.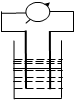 在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
 在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )| M | N | P | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 铜 | 铁 | 硝酸铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
20.下列实验装置设计与对应结论正确的是( )
| 选项 | A | B | C | D |
| 装置 |  | 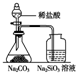 | 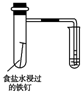 | 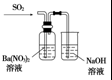 |
| 结论 | 能证明Al(OH)3不溶于氨水 | 能证明非金属性:Cl>C>Si | 验证铁发生析氢腐蚀 | 洗气瓶中产生的白色沉淀是BaSO3 |
| A. | A | B. | B | C. | C | D. | D |
7.下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题.
(1)非金属性最强的元素是F(填元素符号,下同),形成化合物种类最多的元素是C.
(2)画出⑨元素的原子结构示意图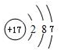 .②的氢化物含有化学键的类型是共价键,与②的氢化物分子所含电子总数相等的分子是H2O(举一例、填化学式,下同)、离子是OH-.
.②的氢化物含有化学键的类型是共价键,与②的氢化物分子所含电子总数相等的分子是H2O(举一例、填化学式,下同)、离子是OH-.
(3)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
(4)⑤⑥⑦单质的活泼性顺序为Na>Mg>Al (填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度Na>Mg>Al(写出一种).
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)画出⑨元素的原子结构示意图
 .②的氢化物含有化学键的类型是共价键,与②的氢化物分子所含电子总数相等的分子是H2O(举一例、填化学式,下同)、离子是OH-.
.②的氢化物含有化学键的类型是共价键,与②的氢化物分子所含电子总数相等的分子是H2O(举一例、填化学式,下同)、离子是OH-.(3)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
(4)⑤⑥⑦单质的活泼性顺序为Na>Mg>Al (填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度Na>Mg>Al(写出一种).
17.如图为氢氧燃料电池原理示意图,下列叙述不正确的是( )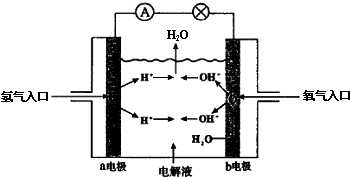

| A. | a电极是负极 | B. | b电极上发生氧化反应 | ||
| C. | 该电池工作时化学能转化为电能 | D. | 该电池的总反应为2H2+O2═2H2O |
1.新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列能源不属于新能源的是( )
| A. | 氢能 | B. | 煤 | C. | 太阳能 | D. | 生物质能 |
2.在玻璃中加入溴化银(AgBr)和氧化铜可制得变色镜片,其中所含物质及变色原理如图所示,下列说法不正确的是( )


| A. | 溴化银应避光保存 | |
| B. | 变色镜片可反复变色 | |
| C. | 变色镜片颜色变深的过程发生了化合反应 | |
| D. | 变色镜片中的氧化铜在变色过程中质量不变 |
 化学反应原理在生活和工业中应用广泛.
化学反应原理在生活和工业中应用广泛.
 .
.