��Ŀ����
�ں���Cu(NO3)2��Zn(NO3)2��Fe(NO3)3��AgNO3��0��1 mol�Ļ����Һ�м���0��1 mol���ۣ���ֽ��������ȫ��Ӧ������Һ�в�����Fe3����ͬʱ������0��1 mol Ag�������н����в���ȷ���ǣ�������
| A����Ӧ����Һ��Cu2����Fe2�������ʵ���֮��Ϊ1��2 |
| B�������ԣ�Ag��>Cu2��>Fe3��>Zn2�� |
| C����Fe3������Һ�ɸ�ʴͭ�� |
| D��1 mol Fe�ɻ�ԭ2 mol Fe3�� |
B
��������������������֪��Fe��ȫ��Ӧ����Fe3����Ag������ȫ��Ӧ��
2Ag��������Fe=Fe2����2Ag��2Fe3��������Fe=3Fe2��
0��1 mol 0��05 mol 0��1 mol 0��05 mol
��֪1 mol Fe�ɻ�ԭ2 mol Fe3����D����ȷ��Cu2����Zn2����δ�μӷ�Ӧ��Fe3����������ǿ��Cu2����Fe3����������ʴͭ�壬B���ȷ��C����ȷ������ԭ���غ㣬��֪��Ӧ����Һ��n(Fe2��)��0��2 mol����n(Cu2��)��n(Fe2��)��0��1 mol��0��2 mol��1��2��A����ȷ��
���㣺���⿼��������ԭ��Ӧԭ�������㡣

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д���ѧ�ϣ�ͨ�����л��ϼ۱仯�ķ�Ӧ����������ԭ��Ӧ�����з�Ӧ����������ԭ��Ӧ���ǣ� ��
| A��CO2+H2O=H2CO3 |
B��2H2O2 2H2O+O2�� 2H2O+O2�� |
C��CaCO3 CO2��+ CaO CO2��+ CaO |
| D��CuSO4+2NaOH ��Cu��OH��2��+Na2SO4 |
��5.6 g Fe���м��������ϡ������Һ������Ӧ��ȫ���ټ���1mol��L-1 KNO3��Һ25mL��ǡ�÷�Ӧ��ȫ���÷�Ӧ�ķ���ʽΪ��
FeSO4 +KNO3 +H2SO4��K2SO4 +Fe2(SO4)3+NxOy + H2O��δ��ƽ������Ը÷�Ӧ������˵����ȷ����
| A����ѧ����ʽ�а�����˳��ļ������ǣ�8��2��5��1��4��1��5 |
| B����Ӧ������������N2O |
| C����Ӧ������ת�Ƶĵ�����Ϊ8mol���� |
| D����������ͻ�ԭ��������ʵ���֮��Ϊ4��1 |
��һδ��ɵ����ӷ���ʽ������+ XO3-+6H+�T3X2+3H2O���ݴ��ж�XԪ�ص�����ϼ�Ϊ
| A��+7 | B��+6 | C��+5 | D��+1 |
������ѧ������ܻ�ù�����߿�ѧ���������Ա�������ϡ����ȡ���۷��������Ĺ��ס���֪�������棨ϡ��Ԫ�أ��ڿ������������䰵������ʱȼ�գ���ˮ�ܿ췴Ӧ����ע���泣���Ļ��ϼ�Ϊ+3��+4�������ԣ�Ce4+>Fe3+>I2��������˵����ȷ����
A�������������Ļ�ѧ����ʽ�ɱ�ʾΪ��Ce + 4HI  CeI4 + 2H2�� CeI4 + 2H2�� |
| B����Ce(SO4)2��Һ�ζ�����������Һ�������ӷ���ʽΪ��Ce4+ + 2Fe2+=Ce3+ + 2Fe3+ |
| C����һ�������£��������״̬��CeO2��Ce������������� |
D��������ֺ���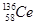 �� �� �� ��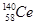 �� �� �����ǻ���Ϊͬ�������� �����ǻ���Ϊͬ�������� |
��֪����ʵ����ʵ����Cr2O3�����������KOH��Һ�õ�KCrO2��Һ��������������õ�Cr2(SO4)3��Һ���ڽ�K2Cr2O7��Һ�μӵ����ۺ�KI�Ļ����Һ�У���Һ����������KCrO2��Һ�еμ�H2O2��Һ�����ữ���ɵ�K2Cr2O7��Һ�������жϲ���ȷ����
| A��������KCrO2��CrԪ��Ϊ+3�� | B��ʵ���֤��Cr2O3������������ |
| C��ʵ���֤�������ԣ�Cr2O72����I2 | D��ʵ���֤��H2O2�������������л�ԭ�� |
�����£���H2O2��Һ�еμ�����FeSO4��Һ���ɷ�������������Ӧ��
2Fe2����H2O2��2H��=2Fe3����2H2O 2Fe3����H2O2=2Fe2����O2����2H��
����˵������ȷ���ǣ�������
| A��H2O2�������Ա�Fe3��ǿ���仹ԭ�Ա�Fe2���� |
| B���ڷ�Ӧ�����У���Һ��pH�������� |
| C���ڷ�Ӧ�����У�Fe2����Fe3�����������ֲ��� |
| D��H2O2��������Ҫ�ϸ�������Fe2�� |
Na2FeO4��һ�ָ�Ч���ˮ��������Ӧ��ǰ��ʮ�ֿ��á�һ���Ʊ�Na2FeO4�ķ�������
��ѧ����ʽ��ʾ���£�2FeSO4 + 6Na2O2�� 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2��
�Դ˷�Ӧ����˵������ȷ���ǣ� ��
| A��Na2O2ֻ�������� | B��Na2FeO4���������������ǻ�ԭ���� |
| C��O2�ǻ�ԭ���� | D��2 mol FeSO4������Ӧʱ����Ӧ�й���8 mol����ת�� |
��֪��������Һ�еĻ�ԭ��ǿ��˳��Ϊ��SO2 ��I�C��H2O2��Fe2����Cl�C�����з�Ӧ�����ܷ������ǣ�
| A��H2O2+ H2SO4��SO2��+ O2��+2 H2O |
| B��2I�C +2Fe3����I2+2 Fe2�� |
| C��2Fe3��+ SO2 +2H2O��2Fe2��+SO42�C +4H�� |
| D��SO2 +2 H2O+ I2��H2SO4+2HI |