题目内容
有一未完成的离子方程式:□□+ XO3-+6H+═3X2+3H2O,据此判断X元素的最高化合价为
| A.+7 | B.+6 | C.+5 | D.+1 |
A
解析试题分析:方程式右边电荷为0,根据离子方程式左右电荷相等,则方程式左边未知物应含有5个负电荷,根据方程式遵循质量守恒定律原子守恒可知,如生成3molX2,则XO3-为1mol,未知物为5mol,所以1mol未知物含有1mol负电荷,离子方程式为:5X-+XO3-+6H+═3X2+3H2O,X的最低化合价为-1价,则X原子核外最外层有7个电子,最高化合价为+7价,故选:A。
考点:常见元素的化合价

 培优口算题卡系列答案
培优口算题卡系列答案现有含0.1 mol/L的SO32-溶液30 mL,恰好被2×10-3 mol XO4-氧化为SO42-,则元素X在还原产物中的化合价是
| A.+4 | B.+3 | C.+2 | D.+1 |
将反应 4(NH4)2SO4→ N2↑+6NH3↑+3SO2↑+SO3↑+7H2O 的产物气体通入BaCl2溶液,下列判断正确的是
| A.无沉淀生成 | B.肯定没有BaSO3生成 |
| C.得到的沉淀是纯净物 | D.得到的沉淀是BaSO4和BaSO3组成的混合物 |
PbO2是褐色固体,受热分解为Pb的+4和+2+4价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3∶2,则剩余固体的组成及物质的量比是
| A.1∶1混合的Pb3O4、PbO |
| B.1∶2混合的PbO2、Pb3O4 |
| C.1∶4∶1混合的PbO2、Pb3O4、PbO |
| D.4∶1∶1混合的PbO2、Pb3O4、PbO |
有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
| A.氧化剂和还原剂的物质的量之比为1∶8 |
| B.该过程说明Fe(NO3)2溶液不宜加酸酸化 |
| C.每1 mol NO3-发生氧化反应,转移8 mol e- |
| D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ |
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学方程式为2KMnO4+10FeSO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,
则下列有关说法中不正确的是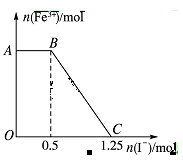
| A.图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D.向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3和AgNO3各0.1 mol的混合溶液中加入0.1 mol铁粉,充分搅拌后铁完全反应,且溶液中不存在Fe3+,同时又析出0.1 mol Ag。则下列结论中不正确的是( )
| A.反应后溶液中Cu2+与Fe2+的物质的量之比为1∶2 |
| B.氧化性:Ag+>Cu2+>Fe3+>Zn2+ |
| C.含Fe3+的溶液可腐蚀铜板 |
| D.1 mol Fe可还原2 mol Fe3+ |
氯气与冷的氢氧化钠反应生成NaCl与NaClO,与热的氢氧化钠反应生成NaCl与NaClO3。一定温度下,氯气与氢氧化钠反应生成的NaClO与NaClO3的物质的量之比为2:3,求该反应氧化产物与还原产物的物质的量之比为( )
| A.5/16 | B.5/17 | C.5/13 | D.13/5 |
已知X和Y是两种单质,X+Y→X2++Y2-,现有下列叙述正确的是: ①X被氧化,②X是氧化剂,③Y2-是还原产物,④X2+具有氧化性,⑤Y2-具有还原性,⑥Y单质氧化性比X2+氧化性强( )
| A.①②③ | B.①②⑥ | C.①③④⑤⑥ | D.①③④⑤ |