题目内容
【题目】图1所示的氮循环是生态系统物质循环的重要组成部分,人类活动加剧了氮循环中的物质转化。
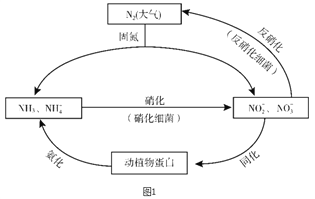
(1)结合上图判断下列说法正确的是________(填字母序号)。
A. 固氮过程中,N2只做氧化剂
B. 在硝化细菌作用下发生的硝化过程需要有氧化剂参与
C. 反硝化过程有助于弥补人工固氮对氮循环造成的影响
D. 同化、氨化过程中,氮元素均从无机物转移至有机物
(2)硝化过程中,NH3转化成HNO2的反应的化学方程式为_______。
(3)反硝化过程中,CH3OH可作为反应的还原剂,请将该反应的离子方程式补充完整:5CH3OH + 6NO3- ![]() N2↑ + 4HCO3- +□______+□
N2↑ + 4HCO3- +□______+□
(4)利用下表数据进行估算,写出工业合成氨反应的热化学方程式:_______。
共价键 | N≡N | H—H | N—H |
断开1mol共价键所需能量(kJ) | 946 | 436 | 391 |
(5)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图2和图3所示。
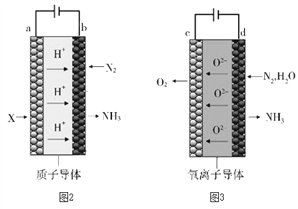
①图2中,a电极上通入的X为_______。
②图3中,d电极上的电极反应式为_______。
③若图2和图3装置的通电时间相同、电流强度相等,电解效率分别为80%和60%,则两种装置中产生氨气的物质的量之比为_______。
【答案】 BC 2NH3 + 3O2 ![]() 2HNO2 + 2H2O 5CH3OH + 6NO3-
2HNO2 + 2H2O 5CH3OH + 6NO3- ![]() 3N2↑ + 4HCO3- + CO32- + 8H2O N2(g) + 3H2(g)
3N2↑ + 4HCO3- + CO32- + 8H2O N2(g) + 3H2(g) ![]() 2NH3(g) ΔH= -92 kJ·mol-1 H2 N2 + 3H2O + 6e-
2NH3(g) ΔH= -92 kJ·mol-1 H2 N2 + 3H2O + 6e- ![]() 2NH3 + 3O2- 4∶3
2NH3 + 3O2- 4∶3
【解析】(1)A. 根据图示,固氮过程中,N2可以转化为氨气,也可以转化为NO3-,氮气既可以做氧化剂,也可以做还原剂,故A错误;B. 在硝化细菌作用下,氨气发生硝化反应生成NO3-,氨气被氧化,需要有氧化剂参与,故B正确;C. 固氮过程中,N2可以转化为氨气,也可以转化为NO3-,反硝化过程中又将NO3-转化为氮气,有助于弥补人工固氮对氮循环造成的影响,故B正确;D. 氨化过程中,将无机物氨气转化为蛋白质等有机物,故D错误;故选BC;
(2)硝化过程中,NH3转化成HNO2的反应的化学方程式为2NH3 + 3O2 = 2HNO2 + 2H2O,故答案为:2NH3 + 3O2 = 2HNO2 + 2H2O;
(3)反硝化过程中,CH3OH可作为反应的还原剂,反应的离子方程式为5CH3OH + 6NO3- ![]() 3N2↑ + 4HCO3- + CO32- + 8H2O,故答案为:5CH3OH + 6NO3-
3N2↑ + 4HCO3- + CO32- + 8H2O,故答案为:5CH3OH + 6NO3- ![]() 3N2↑ + 4HCO3- + CO32- + 8H2O;
3N2↑ + 4HCO3- + CO32- + 8H2O;
(4)工业合成氨反应的化学方程式为N2+ 3H2 ![]() 2NH3,△H=反应物总键能-生成物总键能=946 kJ·mol-1+3×436 kJ·mol-1-6×391 kJ·mol-1= -92 kJ·mol-1,故答案为:N2(g) + 3H2(g)
2NH3,△H=反应物总键能-生成物总键能=946 kJ·mol-1+3×436 kJ·mol-1-6×391 kJ·mol-1= -92 kJ·mol-1,故答案为:N2(g) + 3H2(g) ![]() 2NH3(g) ΔH= -92 kJ·mol-1;
2NH3(g) ΔH= -92 kJ·mol-1;
(5)①根据图示,a为阳极,氢气失去电子生成氢离子,故答案为:氢气;
②图3中,d电极为阴极,氮气和水得到电子生成氨气和O2-,电极反应式为N2 + 3H2O + 6e- = 2NH3 + 3O2-,故答案为:N2 + 3H2O + 6e- = 2NH3 + 3O2-;
③若图2和图3装置的通电时间相同、电流强度相等,电解效率分别为80%和,图2中阳极H2—2e-=2H+,图3中阴极N2 + 3H2O + 6e- = 2NH3 + 3O2-,生成1mol氨气,转移3mol电子,则转移相同的电子,生成的氨气的物质的量之比80%:60%=4:3,故答案为:4:3。

 阅读快车系列答案
阅读快车系列答案