��Ŀ����
�о�CO2��CH4����Ӧʹ֮ת��ΪCO��H2���Լ���ȼ��Σ������С����ЧӦ������Ҫ�����塣
��1����֪��2CO��g��+O2��g����2CO2��g�� ��H����566kJ/mol
2H2��g��+O2��g����2H2O��g�� ��H����484kJ/mol
CH4��g��+2O2��g����CO2��g��+2H2O��g�� ��H����890kJ/mol
��CH4��g��+CO2��g����2CO��g��+2H2��g����H��____________��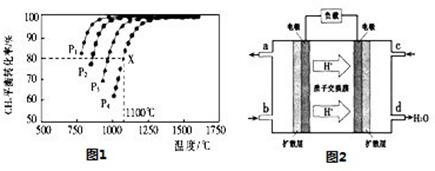
(2)���ܱ�������ͨ�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��CH4��CO2����һ�������·�����ӦCH4��g��+CO2��g����2CO��g��+2H2��g�������CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ1��
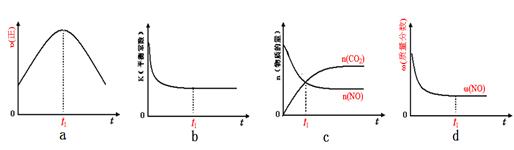
��������ʵ��˵���÷�Ӧһ���ﵽƽ����� ��
a��CO2��Ũ�Ȳ��ٷ����仯
b��������CH4����2������CO��
c����������ƽ����Է��������������仯
d��CO��H2�����ʵ�����Ϊ1:1
�ھ�ͼ��֪��P1��P2��P3��P4�ɴ�С��˳��Ϊ ��
����ѹǿΪP4��1100��������£��÷�Ӧ5minʱ�ﵽƽ��x�㣬����CO��ʾ�÷�Ӧ������Ϊ �����¶��£���Ӧ��ƽ�ⳣ��Ϊ ��
(3)��CO��H2�ɺϳɼ״�(CH3OH)���Լ״���������Ӧ�Ƴɵ�ȼ�ϵ����ͼ2��ʾ���õ�ع�������O2Ӧ�� (�c��һb��)��ͨ�ˣ���ظ�����ӦʽΪ �����øõ�ص�⾫��ͭ��ÿ�õ�6. 4gͭ��ת�Ƶ�����ĿΪ ��
��16�֣���1����160kJ/mol��2�֣� ��2����a��c��2�֣� ��P4��P3��P2��P1��2�֣�
��0.032mol/(L?min)��1.64��2�֣�
��3��c��2�֣���CH3OH��H2O��12e����CO2����6H+��2�֣���1.204��1023��0.2NA��2�֣�
���������������1����֪����2CO��g��+O2��g����2CO2��g�� ��H����566kJ/mol����2H2��g��+O2��g����2H2O��g�� ��H����484kJ/mol����CH4��g��+2O2��g����CO2��g��+2H2O��g�� ��H����890kJ/mol����˸��ݸ�˹���ɿ�֪���ۣ��٣��ڼ��÷�ӦCH4��g��+CO2��g����2CO��g��+2H2��g�������Ը÷�Ӧ�ķ�Ӧ�ȡ�H����890kJ/mol��566kJ/mol��484kJ/mol����160kJ/mol��
��1������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬�����ݷ���ʽCH4��g��+CO2��g����2CO��g��+2H2��g����֪���÷�Ӧ���������Ŀ��淴Ӧ����a��ƽ��ʱ��Ӧ��������ֵ�Ũ�Ȳ��䣬CO2��Ũ�Ȳ��ٷ����仯��˵������ƽ�⣬��a��ȷ��b������(CH4)��2����(CO)�������(CH4):����(CO)��2:1�������ڻ�ѧ������֮�ȣ�δ����ƽ��״̬������Ӧ���ʴ����淴Ӧ���ʣ�ƽ��������Ӧ���У���b����c���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ����Ӧ���������������䣬�淴Ӧ���У���Ӧ�������ܵ����ʵ�������ƽ����Է���������С����������ƽ����Է��������������仯��˵������ƽ�⣬��c��ȷ��d��CO��H2�Ļ�ѧ������Ϊ1:1����Ӧ��ֵ�����ʵ�����Ϊ1:1���У�����˵������ƽ�⣬��d����ѡac��
�ڸ���ͼ��֪���¶�һ��ʱ�������ת���ʦ�(P1)����(P2)����(P3)����(P4)�����ڸ÷�Ӧ����Ӧ�������������ķ�Ӧ������ѹǿƽ�����淴Ӧ���У������ת���ʽ��ͣ���ѹǿP1��P2��P3��P4�ɴ�С��˳��ΪP4��P3��P2��P1��
�۸���ͼ1��֪��ѹǿΪP4��1100��������£��÷�Ӧ5minʱ�ﵽƽ��X�㣬��ʱ�����ת����Ϊ80%����˼����Ũ�ȱ仯��Ϊ0.1mol/L��80%��0.08mol/L����v(CH4)��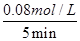 ��0.016mol/(L?min)����������֮�ȵ��ڻ�ѧ������֮�ȿ�֪��v(CO)��2v v(CH4)��2��0.016mol/(L?min)��0.032mol/(L?min)��
��0.016mol/(L?min)����������֮�ȵ��ڻ�ѧ������֮�ȿ�֪��v(CO)��2v v(CH4)��2��0.016mol/(L?min)��0.032mol/(L?min)��
CH4��g��+CO2��g����2CO��g��+2H2��g��
��ʼŨ�ȣ�mol/L�� 0.1 0.1 0 0
ת��Ũ�ȣ�mol/L�� 0.08 0.08 0.16 0.16
ƽ��Ũ�ȣ�mol/L�� 0.02 0.02 0.16 0.16
���Ը��¶���ƽ�ⳣ��K��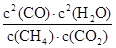 ��
��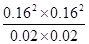 ��1.64
��1.64
��3����ͼ2��֪�������������ת�Ƶ��ұߣ�������������ɣ�����߷���������Ӧ���ұ߷�����ԭ��Ӧ����Ӧ�������õ����ӣ�������ԭ��Ӧ����������c��ͨ�룬�缫�ܷ�ӦʽΪ 2CH3OH��3O2��2CO2����4H2O�������缫��ӦʽΪ3O2��12H+��12e����6H2O���ܷ�Ӧʽ��ȥ������Ӧʽ�ɵø����缫��ӦʽΪ��CH3OH��H2O��12e����CO2����6H+��ͭ�����ʵ���Ϊ6.4g��64g/mol��0.1mol�����ݵ���ת���غ��֪��ת�Ƶ��ӵ���ͭ����ת��Ϊͭ��õĵ��ӣ���ת�Ƶ�����ĿΪ0.1mol��2��NAmol��1��0.2NA��
���㣺�����˹���ɵ�Ӧ�ã�ƽ��״̬���жϡ����������ƽ��״̬��Ӱ�죻��Ӧ���ʺ�ƽ�ⳣ���ļ��㣻�绯ѧԭ����Ӧ���Լ��йؼ����

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д���15�֣��������糧�ͷų������������NOx����SO2��CO2���������ɻ������⡣��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
��1�����������ü������ԭNOx��
CH4(g) �� 4NO2(g) ��4NO(g) �� CO2(g) �� 2H2O(g) ��H1����574 kJ��mol��1
CH4(g) �� 4NO(g) ��2N2(g) �� CO2(g) �� 2H2O(g) ��H2����1160 kJ��mol��1
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ ��
��2����̼����CO2ת��Ϊ�״���CO2(g)��3H2(g) CH3OH(g)��H2O(g) ��H3
CH3OH(g)��H2O(g) ��H3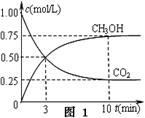
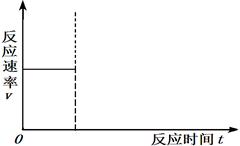
����һ���º����ܱ������г���1 mol CO2��3 mol H2����������Ӧ�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ1��ʾ���ش�0~10 min�ڣ�������ƽ����Ӧ����Ϊ mol/(L��min)����10 min�����¶Ȳ��䣬����ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)����ƽ�� ������������������ƶ���
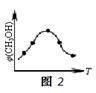
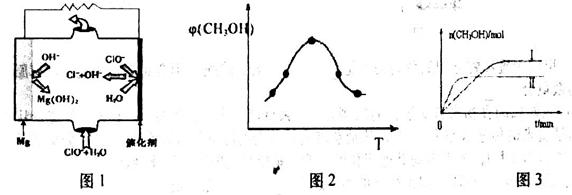
��ȡ��ݵ������CO2��H2�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״�����������գ�CH3OH���뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״��ķ�Ӧ�ġ�H3 0�����������������������
��3����������Na2SO3��Һ���ѳ������е�SO2��Na2SO3����NaOH��Һ����SO2�Ƶá�NaOH��Һ����SO2�Ĺ����У�pH��n(SO32-)�Un(HSO3��)�仯��ϵ���±���
| n(SO32��)�Un(HSO3��) | 91�U9 | 1�U1 | 9�U91 |
| pH | 8.2 | 7.2 | 6.2 |
�� ����Һ������ʱ������Ũ�ȹ�ϵ��ȷ���ǣ�ѡ����ĸ��������������
a��c(Na+)=2c(SO32-)+c(HSO3-)
b��c(Na+) > c(HSO3-) > c(SO32-) > c(H+) = c(OH-)
c��c(Na+) + c(H+) = c(SO32-) + c(HSO3-) + c(OH-)
��14�֣��������ı仯�ͷ�Ӧ�Ŀ����ȽǶ��о���Ӧ��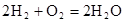 ��
��
��1��Ϊ�˼ӿ�����Ӧ���ʣ����Բ�ȡ�Ĵ�ʩ��________������ţ���ͬ����
| A��ʹ�ô��� | B�����������Ũ�� |
| C����߷�Ӧ���¶� | D�����ͷ�Ӧ���¶� |
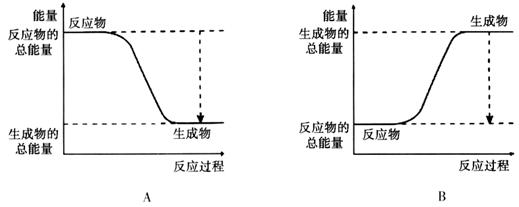
��3���Ӷϼ��ͳɼ��ĽǶȷ���������Ӧ�������ı仯����֪����ѧ���ļ��ܣ�
| ��ѧ�� | H��H | O��O | H��O |
����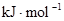 | 436 | 496 | 463 |
��4����֪1��������ȫȼ������Һ̬ˮ�ų�QKJ��������������ȼ������Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽΪ
��5������ȼ�ϵ�ص��ܷ�Ӧ����ʽΪ
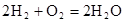 �����У�������________�������������������________��Ӧ�����������ԭ��������·��ÿת��0��2mol���ӣ���״��������H2�������________L��
�����У�������________�������������������________��Ӧ�����������ԭ��������·��ÿת��0��2mol���ӣ���״��������H2�������________L�� ����������ʢ�й���ϡ������Թ��У���Ӱ�������������ʵ�������
| A�������Ũ�� | B�������ı���� | C����Һ���¶� | D��������Na2SO4���� |
 CH3OH(g) ��H��QkJ/mol
CH3OH(g) ��H��QkJ/mol ( CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ����������Ӧ��Q_____0���������������������
( CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ����������Ӧ��Q_____0���������������������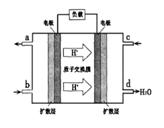
 CH3OH(g) ��H1=��116 kJ��mol��1
CH3OH(g) ��H1=��116 kJ��mol��1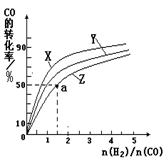
 O2(g)=CO2(g) ��H2=��283 kJ��mol��1
O2(g)=CO2(g) ��H2=��283 kJ��mol��1