题目内容
若某原子的外围电子排布式为4d15s2,则下列说法正确的是
| A.该元素在元素周期表中的位置为第五周期IIIB |
| B.该元素位于s区 |
| C.该元素原子为非金属 |
| D.该元素原子N能层共有8个电子 |
A
解析试题分析:某原子在处于能量最低状态时,外围电子排布为4d15s2,应为钇(Y)元素,位于周期表第五周期第ⅢB族,第N层的电子排布为4s24p64d1。A、外围电子排布为4d15s2,应为钇(Y)元素,位于周期表第五周期第ⅢB族,故A正确;B、区的名称来自于按照构造原理最后填入电子的轨道名称,因此根据外围电子排布为4d15s2可知,处于d区,故B错误;C、该元素属于过渡元素,为金属元素,故C错误;D、第N层的电子排布为4s24p64d1,有9个电子,故D错误,答案选A。
考点:考查核外电子排布以及元素周期表的结构

X、Y、Z、R为前四周期元素且原子序数依次增大。X的单质与氢气可以化合生成气体G,其水溶液pH>7;Y单质是一种黄色固体;R是一种应用最广的金属,它的一种含氧酸根化学式为RO42-,且具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生。Y、Z分别与钠元素可以形成化合物Q和J,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M。则下列说法不正确的是( )
| A.M是离子化合物,且其溶液中阴阳离子个数比为1:l |
| B.L的悬浊液加入Q的溶液,白色沉淀可以转化为黑色沉淀 |
| C.Na2RO4水溶液可以用于杀菌消毒和净水 |
| D.Q的水溶液中加入铝与Z单质形成的化合物,只有白色沉淀生成 |
已知33As、35Br位于同一周期,下列关系正确的是 ( )
| A.原子半径:As>C1>P | B.热稳定性:HC1>AsH3>HBr |
| C.还原性:As3->S2->C1- | D.酸性:H3AsO4>H2SO4>H3PO4 |
关于卤素(F、Cl、Br、I)的化学性质的叙述,错误的是
| A.随原子序数逐渐增大,单质跟水的反应能力逐渐减弱 |
| B.随原子序数逐渐增大,单质的氧化性逐渐减弱 |
| C.将氯水加到KI-淀粉溶液中,溶液变蓝 |
| D.随原子序数逐渐增大,氢化物的稳定性逐渐增强 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是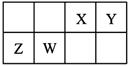
| A.Y元素最高价氧化物对应的水化物化学式为H2YO3 |
| B.原子半径由小到大的顺序为:Y<X<W<Z |
| C.室温下,Z和W的单质均能溶于浓硝酸 |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |
下列事实中,不能用于判断元素失电子能力强弱的是
| A.金属间发生的置换反应 |
| B.金属元素的最高价氧化物对应水化物的碱性强弱 |
| C.金属元素的单质与水或酸反应置换出氢气的难易 |
| D.每摩尔金属单质在反应中失去电子数目的多少 |
下列说法正确的是
| A.金属元素不可能形成含氧酸根离子 |
| B.元素R的含氧酸的化学式是H2RO3,则其气态氢化物的化学式就是RH4 |
| C.金属与非金属元素分界线附近的元素是过渡元素 |
| D.形成化合物种类最多的元素在IVA族 |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |