题目内容
12.有机物A和B均由碳、氢、氧三种元素组成,它们的相对分子质量相等,但碳原子数A比B多两个.2.6g液态A与0.175 mol氧气可恰好完全反应生成0.125 mol CO2和液态水,①生成水的质量为2.7g.②有机物A的分子式为C5H12O,B的分子式为C3H4O4.分析 根据质量守恒求水的质量,所以水的质量为:2.6+0.175×32-0.125×44=2.7g,有机物A中C的物质的量为0.125mol,氢的物质的量为:$\frac{2.7}{18}×2$=0.3mol,所以A分子中氧的物质的量为:0.125×2+0.15×1-0.175×2=0.05mol,所以有机物A中C:H:O=0.125:0.3:0.05=5:12:2,即最简式为C5H12O2,而5个碳12个氢达饱和,所以的分子式为:C5H12O2,结合碳原子数A比B多两个分析解答.
解答 解:①根据质量守恒求水的质量,所以水的质量为:2.6+0.175×32-0.125×44=2.7g,故答案为:2.7g;
②有机物A中C的物质的量为0.125mol,氢的物质的量为:$\frac{2.7}{18}×2$=0.3mol,所以A分子中氧的物质的量为:0.125×2+0.15×1-0.175×2=0.05mol,所以有机物A中C:H:O=0.125:0.3:0.05=5:12:2,即最简式为C5H12O2,而5个碳12个氢达饱和,所以的分子式为:C5H12O2,B比A少两个C,则为3个C,104-36=68,含4个O,4个H,所以分子式为C3H4O4,故答案为:C5H12O;C3H4O4.
点评 本题考查有机物分子式的确定,题目难度中等,确定分子式,首先求出最简式,然后根据饱和度来确定分子式,本题为该类题目的典型.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
3.2015年2月,科学家首次观测到化学键的形成.化学键不存在于( )
| A. | 原子与原子之间 | B. | 分子与分子之间 | C. | 离子与离子之间 | D. | 离子与电子之间 |
7.下列说法不正确的是( )
| A. | 常温下,将CH3COONa溶液,盐酸混合后,溶液呈中性,则有c(Cl-)=c(CH3COOH) | |
| B. | 常温下将pH=2的硫酸和pH=12的氨水等体积混合,所得溶液的pH>7 | |
| C. | pH=3的醋酸溶液加水稀释后,溶液中c(CH3COO-)•c(H+)不变 | |
| D. | 向0.1 mol•L-1的Na2SO3溶液中加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
4.下列有关六方最密堆积与面心立方最密堆积的说法中正确的是( )
| A. | 六方最密堆积是最密堆积,面心立方最密堆积不是最密堆积 | |
| B. | 两者都是最密堆积,其中六方最密堆积是一、三、五…各层球心重合,二、四、六…各层球心重合;面心立方最密堆积是四、五、六…层分别和一、二、三…球心重合 | |
| C. | 原子晶体一般都采用六方最密堆积或面心立方最密堆积 | |
| D. | 只有金属晶体才可能采用六方最密堆积或面心立方最密堆积 |
1.25℃时,0.1mol/L盐酸与0.1mol/L K2CO3溶液等体积混合,下列说法正确的是( )
| A. | 溶液显酸性 | |
| B. | c(H+)+c(K+)=c(OH-)+c(Cl-)+c(HCO3-)+c(CO32-) | |
| C. | c(Cl-)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | c(K+)>c(HCO3-)>c(Cl-)>c(OH-)>c(H+) |
18.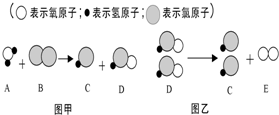 自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:根据以上图示判断下列说法错误的是( )
自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:根据以上图示判断下列说法错误的是( )
 自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:根据以上图示判断下列说法错误的是( )
自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:根据以上图示判断下列说法错误的是( )| A. | 图乙的反应是分解反应 | |
| B. | D物质代表着氧化物 | |
| C. | 图甲的化学反应方程式为:Cl2+H2O═HCl+HClO | |
| D. | 由图乙可总结出:反应前后元素的种类不改变 |

 .
.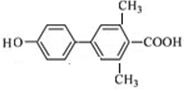 、
、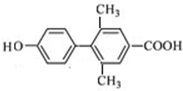 、
、 、
、 (其中一种).
(其中一种).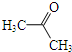 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:

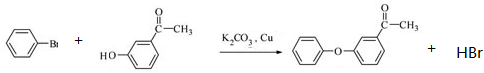
 也可发生类似反应①的反应,生成化合物Ⅳ:
也可发生类似反应①的反应,生成化合物Ⅳ: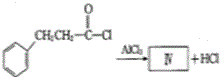
 .
. .
. .
.