题目内容
(10分)下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下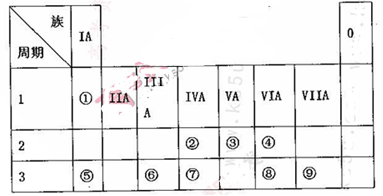
列问题:
(1)画出表中形成化合物种类最多元素的原子结构示意图____;写出它与原予半径最小的原子形成10电子且为正四面体结构的化合物的电子式____,用电子式表示⑤和⑧形成化合物的过程________。
(2).④⑤⑧形成的简单离子半径由大到小的顺序为____(填离子符号);③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为_______(填化学式)。
(3).⑤和⑨形成化合物的化学键为__________。
(4).这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是_______(填化学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式___________________________。
(1)碳的原子结构示意图是 ;甲烷的电子式
;甲烷的电子式 ;
; ;
;
(2)S2->O2->Na+;HClO4>HNO3>H2SiO3
(3)离子键
(4)Al2O3;Al2O3+2OH-=2AlO-2+H2O
解析试题分析:(1)表中形成化合物种类最多元素是③号元素C,核电荷数是6,原子结构示意图是 ;原子半径最小的是①号H元素,C与H形成的10电子的化合物是甲烷,其电子式为
;原子半径最小的是①号H元素,C与H形成的10电子的化合物是甲烷,其电子式为 ;⑤⑧分别是Na、S元素,二者形成离子化合物Na2S,用电子式表示形成过程如下:
;⑤⑧分别是Na、S元素,二者形成离子化合物Na2S,用电子式表示形成过程如下: ;
;
(2)④⑤⑧形成的简单离子分别是O2-、Na+、S2-,S2-的电子层数最多,半径最大,O2-、Na+的电子层数相同,核电荷数越多半径越小,所以Na+的半径最小;根据元素非金属性的强弱,N、Si、Cl的最高价含氧酸的强弱顺序是HClO4>HNO3>H2SiO3
(3)⑤和⑨形成化合物是NaCl,含有离子键;
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是Al2O3;⑤的最高价氧化物对应水化物是NaOH,氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO-2+H2O。
考点:考查对元素周期表的认知,元素及其化合物的性质,元素周期律的应用

现有部分元素的性质与原子(或分子)结构如下表:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
(2)元素Y与元素Z相比,金属性较强的是__________________(用元素符号表示),下列表述中能证明这一事实的是_________________(填序号);
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式___________,并写出该化合物与水反应的离子方程式______;
(4)元素T和氢元素以原子个数比1∶1化合形成的化合物属于______________,元素Z与元素T形成的化合物属于____________________(以上两空选填“共价化合物”或“离子化合物”)。
(8分)下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:
| a | | | |||||
| | | | b | c | d | | |
| e | | f | | | g | | |
(2) e 与f两元素最高价氧化物的水化物相互反应的化学方程式为
_____________________________________________________
(3)e在空气中燃烧的产物所含化学键的类型为__________、__________。
(4) 化合物ca3的电子式为 ,c和d两种元素氢化物的稳定性更强的是 _______(填物质的化学式)。
(13分)下图是元素周期表的一部分,表中的①—⑩中元素,用化学用语填空回答:
| 族 周期 | I A | IIA | IIIA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 二 | | | | ① | ② | | ③ | |
| 三 | | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | | | | | | ⑩ | |
(1)在这些元素中,⑩原子的原子结构示意图为 。
(2)写出①的最高价氧化物和②的单质的电子式 , 。
(3)用电子式表示③与④形成化合物的过程 。
(4)①的单质和⑥的氧化物反应的化学方程式 。
(5)写出⑤的单质与氢氧化钠反应的化学方程式:
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式: 。
(6)已知拆开l mol C—H键、l mol O=O键、l molC=O键、l mol H—O键分别需要吸收的能量为414kJ、498kJ、728kJ、464kJ。则l mol甲烷完全燃烧放出 kJ的热量。
【选修3-物质结构与性质】(20分)
19-I(6分)对于钠的卤化物(NaX)和硅的卤化物(SiX4),下列叙述正确的是
| A.SiX4难水解 | B.SiX4是共价化合物 |
| C.NaX易水解 | D.NaX的熔点一般高于SiX4 |
回答下列问题:
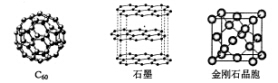
(1)金刚石、石墨、C60.碳纳米管等都是碳元素的单质形式,它们互为_____________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为____、____。
(3)C60属于____晶体,石墨属于____晶体。
(4)石墨晶体中,层内C-C键的键长为142 pm,而金刚石中C-C键的键长为154 pm。其原因是金刚石中只存在C-C间的____共价键,而石墨层内的C-C间不仅存在____共价键,还有____键。
(5)金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______a,列式表示碳原子在晶胞中的空间占有率____(不要求计算结果)。
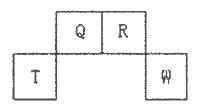

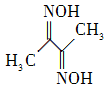
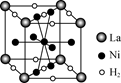
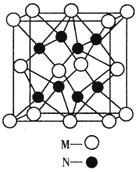
 cm,则距离最近的M、N离子间的距离为
cm,则距离最近的M、N离子间的距离为