题目内容
常温下,对于醋酸溶液的下列说法中,不正确的是
| A.0.1 mol·L-1的醋酸溶液中加水稀释,溶液中c(OH-)减小 |
| B.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| C.pH=4的醋酸溶液与pH=10的烧碱溶液等体积混合后溶液呈酸性 |
| D.醋酸溶液中加入少量醋酸钾晶体,醋酸电离程度减小 |
A
醋酸是弱酸,存在电离平衡,稀释促进电离,但氢离子的浓度降低,所以c(OH-)增大,A不正确。C符合电荷守恒,正确。pH=4的醋酸溶液的浓度大于0.0001mol/L,所以反应中醋酸是过量的,溶液显酸性,C正确。增大醋酸根离子的浓度抑制醋酸的电离,D正确,答案选A。

练习册系列答案
相关题目
 浓度最大的是
浓度最大的是

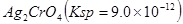

 CH3OH(g)
CH3OH(g) 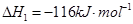
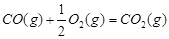
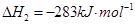
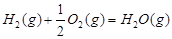
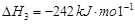
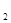 和水蒸气的热化学方程式为 。
和水蒸气的热化学方程式为 。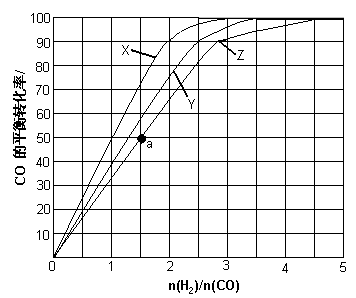
 Ca2+(aq)+2OH-(aq),下列叙述正确的是
Ca2+(aq)+2OH-(aq),下列叙述正确的是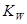 ,该温度下将a mol?L-1一元酸HA与b mol?L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是
,该温度下将a mol?L-1一元酸HA与b mol?L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是