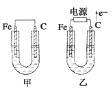
题目内容
【题目】有机物K是某药物的前体,合成路线如图所示:
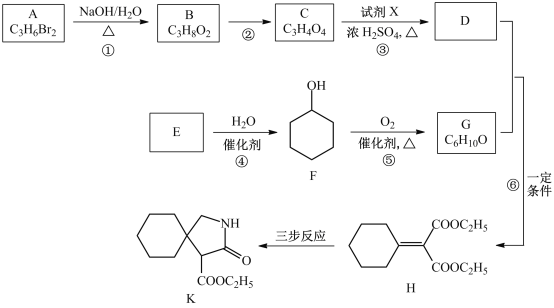
已知:R-CN![]()
![]() ;
;
![]()
![]() +
+![]()
(1)A的名称是_____________。
(2)反应①的化学方程式是___________________。
(3)反应②的类型是__________________。
(4)反应③中的试剂X是________________。
(5)E属于烃,其结构简式是_________________。
(6)H中所含的官能团是_________________。
(7)反应⑥的化学方程式是_____________________。
(8)H经三步反应合成K,写出中间产物I和J的结构简式______________。
![]()
【答案】1,3-二溴丙烷 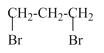 +2NaOH
+2NaOH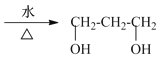 +2H2O 氧化反应 乙醇
+2H2O 氧化反应 乙醇 ![]() 碳碳双键,酯基
碳碳双键,酯基 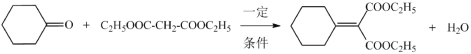 I:
I: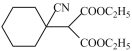 J:
J: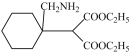
【解析】
由题可知,A是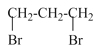 ,B是
,B是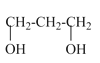 ,C是
,C是![]() ,D是
,D是![]() ,E是
,E是![]() ,F是
,F是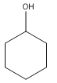 ,G是
,G是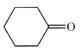 。
。
(1)由分析可知,A是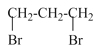 ,则A的名称是:1,3-二溴丙烷;
,则A的名称是:1,3-二溴丙烷;
(2)反应①是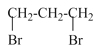 水解成
水解成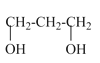 ,则化学方程式为
,则化学方程式为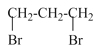 +2NaOH
+2NaOH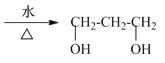 +2H2O;
+2H2O;
(3)反应②是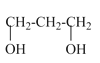 经强氧化剂氧化成
经强氧化剂氧化成![]() ,则反应类型是氧化反应;
,则反应类型是氧化反应;
(4)反应③是![]() 经酯化反应生成
经酯化反应生成![]() ,可知试剂X是乙醇;
,可知试剂X是乙醇;
(5)由分析可知,E结构简式是![]() ,属于烃;
,属于烃;
(6)H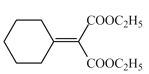 中所含的官能团是碳碳双键,酯基;
中所含的官能团是碳碳双键,酯基;
(7)反应⑥是 与
与![]() 发生取代反应生成
发生取代反应生成 ,其化学方程式为
,其化学方程式为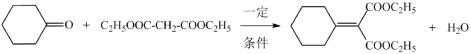 ;
;
(8)由已知信息可知,H 先与HCN加成生成I:
先与HCN加成生成I: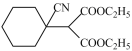 ,I再与氢气加成生成J:
,I再与氢气加成生成J: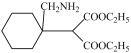 ,J再在催化剂条件下反应生成
,J再在催化剂条件下反应生成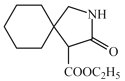 。
。

练习册系列答案
相关题目