��Ŀ����
����Ŀ��NO2��N2O4���ת��2NO2(g)![]() N2O4(g)�Ǹ���������ѧ���ۻ�ѧƽ������ij�����ϵ����ش�
N2O4(g)�Ǹ���������ѧ���ۻ�ѧƽ������ij�����ϵ����ش�
��.��N2O4 (g)ת��ΪN2O4(l)���������Ʊ����ᡣ
(1)��֪2NO2(g)![]() N2O4(g) ��H1 2NO2(g)
N2O4(g) ��H1 2NO2(g)![]() N2O4(l) ��H2
N2O4(l) ��H2
���������仯ʾ��ͼ��ȷ����__________��
A��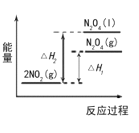 B��
B��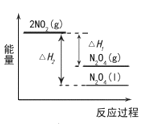 C��
C��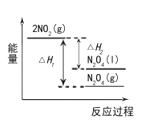
(2)NO2��N2O4���ʵ���֮��Ϊ1:1��O2��H2Oǡ����ȫ��Ӧ�Ļ�ѧ����ʽΪ__________��
��.����2NO2(g)![]() N2O4(g)��Ӧ��ϵ����ƽ�ⳣ��K��=
N2O4(g)��Ӧ��ϵ����ƽ�ⳣ��K��=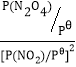 ������P��Ϊ��ѹǿ(1��105 Pa)��P(N2O4)��P(NO2)Ϊ�����ƽ���ѹ(ƽ���ѹ=��ѹ�����ʵ�������)��
������P��Ϊ��ѹǿ(1��105 Pa)��P(N2O4)��P(NO2)Ϊ�����ƽ���ѹ(ƽ���ѹ=��ѹ�����ʵ�������)��
(1)����ʼNO2�����ʵ�����Ϊ1mol����Ӧ�ں㶨�¶Ⱥͱ�ѹǿ�½��У�N2O4��ƽ�����Ϊ0.75����K��=____________��
(2)�����ִ��ֳּ�������������̽��ѹǿ��2NO2(g)![]() N2O4(g)��ѧƽ���ƶ���Ӱ�졣�ں㶨�¶Ⱥͱ�ѹǿ�����£�����Ͳ�г���һ�������NO2������ܷⲢ���ֻ���λ�ò��䡣�ֱ���t1��t2ʱ��Ѹ���ƶ��������ֻ���λ�ò��䣬�ⶨ��Ͳ������ѹǿ�仯��ͼ��ʾ��
N2O4(g)��ѧƽ���ƶ���Ӱ�졣�ں㶨�¶Ⱥͱ�ѹǿ�����£�����Ͳ�г���һ�������NO2������ܷⲢ���ֻ���λ�ò��䡣�ֱ���t1��t2ʱ��Ѹ���ƶ��������ֻ���λ�ò��䣬�ⶨ��Ͳ������ѹǿ�仯��ͼ��ʾ��
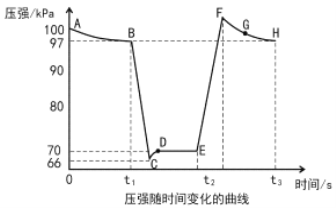
��B��ʱNO2��ת����Ϊ_______��
��E��H�����Ӧ�����ƽ����Է�������ME____MH(������������=��)��
��.�����������(S2O42-)Ϊý�飬ʹ�ü�ӵ绯ѧ��Ҳ�ɴ���ȼú�����е�NO��װ����ͼ��ʾ��

(3)���������ĵ缫��ӦʽΪ_________��
��NO����ת�������Ҫ����ΪNH4+����ͨ��ʱ��·��ת����0.3mole�������ͨ����������������յ�NO�ڱ�״���µ����Ϊ____mL��
��.�����£���a mol��L-1�Ĵ�����bmol��L-1Ba(OH)2��Һ�������ϣ���ַ�Ӧ����Һ�д���2c(Ba2+)=c(CH3COO-)����û����Һ�д���ĵ��볣��Ka=_____(�ú�a��b�Ĵ���ʽ��ʾ)��
���𰸡�B 4NO2+4N2O4+3O2+6H2O=12HNO3 3.75 6% �� 2SO32-��4H����2e��=S2O42-��2H2O 1344 ![]()
��������
��(1)2NO2(g)N2O4(g)Ϊ���ȷ�Ӧ������H1��0�� 2NO2(g)N2O4(l)Ϊ���ȷ�Ӧ������H2��0��N2O4(g)ת��ΪN2O4(l)Ϊ���ȷ�Ӧ����������N2O4(g)��N2O4(l)���ݴ˷����жϣ�(2)������������ת��Ϊ��������������������������ˮ��Ӧ�������ᣬ����Ҫ����д��Ӧ�Ļ�ѧ����ʽ��
��(1)���1mol����������ȫת��Ϊ���������������������������������ʵ���Ϊ0.5mol��N2O4��ƽ�����Ϊ0.75��������n(N2O4)=0.5��0.75mol=0.375mol�����ĵ�n(NO2)=2��0.375mol=0.75mol�����ƽ��ʱ������������ʵ�����ƽ���ѹ=��ѹ�����ʵ������������PN2O4��PNO2�����K��=![]() ���㣻
���㣻
(2)�ٺ��º��������£�����ѹǿ֮�ȵ������ʵ���֮�ȣ��迪ʼʱ�������������ʵ���Ϊ1mol����B�������������ʵ���=![]() ��1mol=0.97mol�����ݷ���ʽ����μӷ�Ӧ��n(NO2)���ټ������������ת���ʣ��ں���ʱѹǿԽ�����������ʵ���Խ��Ӧǰ���������������䣬��������ƽ����Է���������С��
��1mol=0.97mol�����ݷ���ʽ����μӷ�Ӧ��n(NO2)���ټ������������ת���ʣ��ں���ʱѹǿԽ�����������ʵ���Խ��Ӧǰ���������������䣬��������ƽ����Է���������С��
III��(3)�ٸ���ͼ��������ͨ���Һ����Ҫ��SO32-��������Ҫ��S2O42-���ݴ���д�������ĵ缫��Ӧʽ��������NO����ת�������Ҫ����ΪNH4+������ת�Ƶĵ���������յ�NO��
������a mol/L�Ĵ�����b mol/L Ba(OH)2��Һ�������ϣ���Һ������Ϊ���ᱵ��������������Ӧƽ��ʱ��2c(Ba2+)=c(CH3COO-)����Һ��c(H+)=c(OH-)=10-7mol/L����Һ�����ԣ����ݵ��뷽��ʽ�������ĵ���ƽ�ⳣ����
��(1)2NO2(g)N2O4(g)Ϊ���ȷ�Ӧ������H1��0����Ӧ�������������������������� 2NO2(g)N2O4(l)Ϊ���ȷ�Ӧ������H2��0����Ӧ��������������������������N2O4(g)ת��ΪN2O4(l)Ϊ���ȷ�Ӧ����������N2O4(g)��N2O4(l)��ֻ��B���ϣ��ʴ�Ϊ��B��
(2)������������ת��Ϊ��������������������������ˮ��Ӧ�������ᣬNO2��N2O4���ʵ���֮��Ϊ1:1��O2��H2Oǡ����ȫ��Ӧ�Ļ�ѧ����ʽΪ4NO2+4N2O4+3O2+6H2O=12HNO3���ʴ�Ϊ��4NO2+4N2O4+3O2+6H2O�T12HNO3��
��(1)���1mol����������ȫת��Ϊ���������������������������������ʵ���Ϊ0.5mol��N2O4��ƽ�����Ϊ0.75��������n(N2O4)=0.5��0.75mol=0.375mol�����ĵ�n(NO2)=2��0.375mol=0.75mol��ƽ��ʱ������������ʵ���=(0.375+1-0.75)mol=0.625mol��PN2O4=![]() ��P��=0.6P����PNO2=
��P��=0.6P����PNO2=![]() ��P��=0.4P������ƽ�ⳣ��K��=
��P��=0.4P������ƽ�ⳣ��K��=![]() =
=![]() =3.75���ʴ�Ϊ��3.75��
=3.75���ʴ�Ϊ��3.75��
(2)�ٺ��º��������£�����ѹǿ֮�ȵ������ʵ���֮�ȣ��迪ʼʱ�������������ʵ���Ϊ1mol����B�������������ʵ���=![]() ��1mol=0.97mol�����ݷ���ʽ2NO2(g)
��1mol=0.97mol�����ݷ���ʽ2NO2(g)![]() N2O4(g)֪����Ӧǰ����ٵ����ʵ����൱�ڲμӷ�Ӧ�Ķ������������ʵ���һ�룬��μӷ�Ӧ��n(NO2)=(1-0.97)mol��2=0.06mol����������ת����=
N2O4(g)֪����Ӧǰ����ٵ����ʵ����൱�ڲμӷ�Ӧ�Ķ������������ʵ���һ�룬��μӷ�Ӧ��n(NO2)=(1-0.97)mol��2=0.06mol����������ת����=![]() ��100%=6%���ʴ�Ϊ��6%��
��100%=6%���ʴ�Ϊ��6%��
�ں���ʱѹǿԽ�����������ʵ���Խ��Ӧǰ���������������䣬��������ƽ����Է�������ԽС��t1ʱ�����������������ѹǿ��С��ƽ�������ƶ�������������Է���������С��t2��С���������ѹǿ����ƽ�������ƶ����������ʵ�����С����С����H�㣬��H������Է����������ĵ㣬E��H�����Ӧ�����ƽ����Է�������ME��MH���ʴ�Ϊ������
III��(3)����ͼ��֪��������ͨ���Һ����Ҫ��SO32-��������Ҫ��S2O42-�������������缫��ӦʽΪ2SO32-+4H++2e-=S2O42-+2H2O���ʴ�Ϊ��2SO32-+4H++2e-=S2O42-+2H2O��
������NO����ת�������Ҫ����ΪNH4+��NO��NH4+��5e-������·��ת��0.3mol e-��������NO 0.06mol���ڱ�״���µ����Ϊ=0.06mol��22.4L/mol=1.344L=1344mL���ʴ�Ϊ��1344��
����ͨ��״���£���a mol/L�Ĵ�����b mol/L Ba(OH)2��Һ�������ϣ���Һ������Ϊ���ᱵ��������������Ӧƽ��ʱ��2c(Ba2+)=c(CH3COO-)=bmol/L����Һ��c(H+)=c(OH-)=10-7mol/L����Һ�����ԣ��������ƽ�ⳣ�����ݵ��뷽��ʽд��K=![]() =
=![]() =
=![]() ��10-7���ʴ�Ϊ��
��10-7���ʴ�Ϊ��![]() ��10-7��
��10-7��

 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д�����Ŀ�����в���Ԫ�ص�������ԭ��(�����)�ṹ�������Ϣ�����ʾ��
Ԫ�ر�� | Ԫ��������ԭ��(�����)�ṹ�������Ϣ |
T | �����������Ǵ����������� 3 �� |
X | �����µ��ʷ���Ϊ˫ԭ�ӷ��ӣ������к��� 3 �Թ��õ��Ӷ� |
Y | M ���K ���� 1 ������ |
Z | �������ǵ������ڽ���Ԫ�ص������а뾶��С�� |
(1)T��X��Y��Z �γɵļ����Ӱ뾶�ɴ�С��˳����_____��(�����ӷ��ű�ʾ)
(2)Ԫ�� Y ��Ԫ�� Z ��ȣ������Խ�ǿ����_____(��Ԫ�ط��ű�ʾ)�����б������� ֤����һ��ʵ����_____(����ĸ���)��
a.Y ���ʵ��۵�� Z ���ʵĵ�
b.Y �Ļ��ϼ۱�Z �ĵ�
c.������Y ������ˮ��Ӧ�ij̶Ⱥܾ��ң���Z �����ڼ��������²�����ˮ��Ӧ
d.Y ����������Ӧ��ˮ����ļ��Ա� Z ��ǿ
(3)T��X��Y��Z ��������Ԫ�����γɼȺ����Ӽ��ֺ��Ǽ��Թ��ۼ��ij��������д���û�����ĵ���ʽ��________��Ԫ�� X ����Ԫ����ԭ�Ӹ����� 1��2 �����γɳ����ڻ��ȼ�ϵĻ����� W��д�� W �ĵ���ʽ_______
(4)Ԫ�� T ����Ԫ����ԭ�Ӹ����� 1��1 �����γɻ����� Q�� Q ���� W ����������ԭ��Ӧ�� ����X �ĵ��ʺ�T ����һ���⻯�д���÷�Ӧ�Ļ�ѧ����ʽ��_______