题目内容
[选修物质结构与性质](15分)
A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增。已知:B原子核外最外层电子数是次外层电子数的两倍,电子总数是E原子总数的1/2,F是同周期元素中原子半径最小的元素;D2-与E2+的电子层结构相同。B与D可以形成三原子化合物甲。A是非金属元素,且A、C、F可形成离子化合物乙。请回答:
(1)C单质的电子式 ,F元素原子的电子排布式 ,E元素的原子结构示意图是 。
(2)化合物乙中含有的化学键是 。
(3)化合物甲为固体时属于 晶体,E单质在一定条件下与甲反应的化学方程式为  。
。
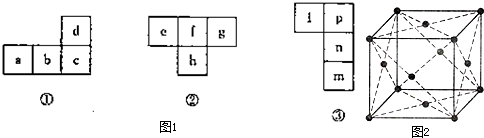
(4)如图立方体中心的“·”表示B单质所形成的原子晶体中的一个原子,请在立方体的顶点用“·”表示出与之紧邻的B原子
(1)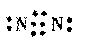 1s22s22p63s23p5
1s22s22p63s23p5  (6分)
(6分)
(2)离子键、共价键和配位键(3分)
(3)分子 2Mg+CO2
(4)(3分)
解析

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
 (2012?长春三模)[化学-选修 物质结构与性质]A、B、C、D、E、F为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子核外电子有7种运动状态,B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2形化合物,F原子核外最外层只有1个电子,其余各层均充满电子.
(2012?长春三模)[化学-选修 物质结构与性质]A、B、C、D、E、F为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子核外电子有7种运动状态,B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2形化合物,F原子核外最外层只有1个电子,其余各层均充满电子.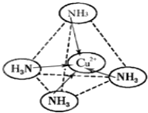
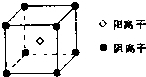 其电子式为
其电子式为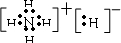
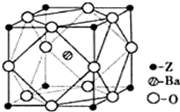 [化学-选修物质结构与性质]
[化学-选修物质结构与性质]