��Ŀ����
 ��2012?������ģ��[��ѧ-ѡ�� ���ʽṹ������]A��B��C��D��E��FΪԭ�������������������Ԫ�أ���֪��A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B�Ļ�̬ԭ�Ӻ��������7���˶�״̬��B��C��E����Ԫ��ԭ����δ�ɶԵ�����֮��Ϊ3��2��1��Dԭ�Ӻ�����4���ܼ��Ҿ��������ӣ�D��E���γ�DE2�λ����Fԭ�Ӻ��������ֻ��1�����ӣ����������������ӣ�
��2012?������ģ��[��ѧ-ѡ�� ���ʽṹ������]A��B��C��D��E��FΪԭ�������������������Ԫ�أ���֪��A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B�Ļ�̬ԭ�Ӻ��������7���˶�״̬��B��C��E����Ԫ��ԭ����δ�ɶԵ�����֮��Ϊ3��2��1��Dԭ�Ӻ�����4���ܼ��Ҿ��������ӣ�D��E���γ�DE2�λ����Fԭ�Ӻ��������ֻ��1�����ӣ����������������ӣ��ش��������⣺
��1��B��C��D����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ
N��O��Mg
N��O��Mg
������Ԫ�ط��ű�ʾ����2��F�����ڱ���λ��
ds
ds
������۵����Ų�ʽΪ3d104s1
3d104s1
����Fͬ������δ�ɶԵ���������Ԫ��ΪCr
Cr
����дԪ�ط��ţ�����3��B��E����Ԫ���п��γ�XY3�λ�����Ļ�ѧʽΪ
NCl3
NCl3
��������ԭ���ӻ���ʽΪsp3
sp3
�����ӵĿռ乹��Ϊ������
������
����4��A��B�γɵĻ��������ܽ���A��C�γɵĻ������У���ԭ����
�����Ӽ����γ����
�����Ӽ����γ����
����5��DC�������۵����DE2���۵㣬��ԭ����
MgO�ľ����ܸ���MgCl2
MgO�ľ����ܸ���MgCl2
����6��F2+��NH3�γ�������[F��NH3��4]2+����[F��NH3��4]2+�У�F2+λ�������������ģ�NH3λ����������Ķ��㣬����ͼ�б�ʾ[F��NH3��4]2+��F2+��N֮��Ļ�ѧ��
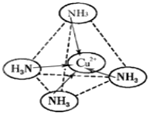

������A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�ӦΪHԪ�أ�B�Ļ�̬ԭ�Ӻ��������7���˶�״̬��˵����7�����ӣ�ΪNԪ�أ�B��C��E����Ԫ��ԭ����δ�ɶԵ�����֮��Ϊ3��2��1�����Ƴ�C��OԪ�أ�����Dԭ�Ӻ�����4���ܼ��Ҿ��������ӣ�D��E���γ�DE2�ͻ�������Ƴ�E��ClԪ�أ�D��Mg������Fԭ�Ӻ��������ֻ��1�����ӣ����������������ӣ����Ƴ�FΪCuԪ�أ���Fͬ������δ�ɶԵ���������Ԫ��ΪCr����϶�ӦԪ�ض�Ӧ�ĵ��ʡ�������������Լ���ĿҪ������⣮
����⣺A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�ӦΪHԪ�أ�B�Ļ�̬ԭ�Ӻ��������7���˶�״̬��˵����7�����ӣ�ΪNԪ�أ�B��C��E����Ԫ��ԭ����δ�ɶԵ�����֮��Ϊ3��2��1�����Ƴ�C��OԪ�أ�����Dԭ�Ӻ�����4���ܼ��Ҿ��������ӣ�D��E���γ�DE2�ͻ�������Ƴ�E��ClԪ�أ�D��Mg������Fԭ�Ӻ��������ֻ��1�����ӣ����������������ӣ����Ƴ�FΪCuԪ�أ���Fͬ������δ�ɶԵ���������Ԫ��ΪCr��
��1��N��O�����ڱ���ͬ���ڣ�N�������Ϊ������ṹ������ʧȥ���ӣ���һ�����ܽϴ�ΪN��O��Mg��
�ʴ�Ϊ��N��O��Mg��
��2��FΪCuԪ�أ��۵����Ų�ʽΪ3d104s1��λ�����ڱ�ds������Fͬ������δ�ɶԵ���������Ԫ��ΪCr��
�ʴ�Ϊ��ds��3d104s1��Cr��
��3��B��E����Ԫ���п��γ�XY3�λ�����Ļ�ѧʽΪNCl3��N�γ�3���ļ�������1���µ��Ӷԣ�Ϊsp3�ӻ������ӵĿռ乹��Ϊ�����Σ�
�ʴ�Ϊ��NCl3��sp3�������Σ�
��4��A��B�γɵĻ�����Ϊ������A��C�γɵĻ�����Ϊˮ�������Ӽ����γ���������°�����������ˮ��
�ʴ�Ϊ�������Ӽ����γ������
��5��MgO�������۵����MgCl2���۵㣬ԭ����MgO�ľ����ܸ���MgCl2��
�ʴ�Ϊ��MgO�ľ����ܸ���MgCl2��
��6��F2+��N֮����γ���λ�����ɱ�ʾΪ ��
��
�ʴ�Ϊ�� ��
��
��1��N��O�����ڱ���ͬ���ڣ�N�������Ϊ������ṹ������ʧȥ���ӣ���һ�����ܽϴ�ΪN��O��Mg��
�ʴ�Ϊ��N��O��Mg��
��2��FΪCuԪ�أ��۵����Ų�ʽΪ3d104s1��λ�����ڱ�ds������Fͬ������δ�ɶԵ���������Ԫ��ΪCr��
�ʴ�Ϊ��ds��3d104s1��Cr��
��3��B��E����Ԫ���п��γ�XY3�λ�����Ļ�ѧʽΪNCl3��N�γ�3���ļ�������1���µ��Ӷԣ�Ϊsp3�ӻ������ӵĿռ乹��Ϊ�����Σ�
�ʴ�Ϊ��NCl3��sp3�������Σ�
��4��A��B�γɵĻ�����Ϊ������A��C�γɵĻ�����Ϊˮ�������Ӽ����γ���������°�����������ˮ��
�ʴ�Ϊ�������Ӽ����γ������
��5��MgO�������۵����MgCl2���۵㣬ԭ����MgO�ľ����ܸ���MgCl2��
�ʴ�Ϊ��MgO�ľ����ܸ���MgCl2��
��6��F2+��N֮����γ���λ�����ɱ�ʾΪ
 ��
���ʴ�Ϊ��
 ��
������������Ӧ��Ԫ�����ڱ����������ƶϳ���Ԫ�أ����Դ˿�����Ԫ�صĵ�һ�����ܣ�Ԫ�ط������۵����Ų�ʽ�����ӵĿռ乹�ͣ�������ԭ�ӵ��ӻ����ͣ�����������ܣ�����ѧ��������߿��ıؿ����ͣ��ѶȲ�����Ĺؼ���Ҫ����������ھ������������Ϣ���硰ԭ�����������������ԭ�ӽṹ�����ӵ��Ų�����������

��ϰ��ϵ�д�
�����Ŀ
 ��2012?������ģ��A��B��C��D������ѧ��ѧ�г������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ��ͼ�����ַ�Ӧ�е�ˮ����ȥ����
��2012?������ģ��A��B��C��D������ѧ��ѧ�г������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ��ͼ�����ַ�Ӧ�е�ˮ����ȥ����