题目内容
下列叙述正确的是( )
| A、非金属原子间以共价键结合的物质都是共价化合物 |
| B、制催化剂的材料和制耐高温、耐腐蚀的合金材料可在过渡元素中寻找 |
| C、1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 |
| D、铷的熔点比钠高,其硫酸盐易溶于水 |
考点:元素周期律和元素周期表的综合应用,中和热
专题:化学反应中的能量变化,元素周期律与元素周期表专题
分析:A.非金属原子之间可以形成单质;
B.优良的催化剂和耐高温、耐腐蚀的合金材料大多属于过渡元素;
C.酸与碱稀溶液发生中和反应生成1mol水时所释放的热量称为中和热;
D.碱金属自上而下金属离子半径增大,金属性减弱,单质的熔点较低.
B.优良的催化剂和耐高温、耐腐蚀的合金材料大多属于过渡元素;
C.酸与碱稀溶液发生中和反应生成1mol水时所释放的热量称为中和热;
D.碱金属自上而下金属离子半径增大,金属性减弱,单质的熔点较低.
解答:
解:A.非金属原子之间以共价键结合的物质可以是共价化合物,也可以是单质,故A错误;
B.在过渡元素中寻找优良的催化剂和耐高温、耐腐蚀的合金材料,故B正确;
C.酸与碱稀溶液发生中和反应生成1mol水时所释放的热量称为中和热,故C错误;
D.碱金属自上而下金属离子半径增大,金属性减弱,单质的熔点较低,故铷的熔点比钠低,故D错误,
故选B.
B.在过渡元素中寻找优良的催化剂和耐高温、耐腐蚀的合金材料,故B正确;
C.酸与碱稀溶液发生中和反应生成1mol水时所释放的热量称为中和热,故C错误;
D.碱金属自上而下金属离子半径增大,金属性减弱,单质的熔点较低,故铷的熔点比钠低,故D错误,
故选B.
点评:本题考查化学键、元素周期表与元素周期律应用、中和热、同主族元素化合物性质相似性与递变性等,比较基础,注意理解中和热:应为稀的酸、碱溶液反应,生成的水为1mol.

练习册系列答案
相关题目
下列对氧化还原反应的叙述,正确的是( )
| A、氧化还原反应中,某元素由化合态变为游离态时,一定被还原 |
| B、阳离子只有氧化性,阴离子只有还原性 |
| C、氧化剂在氧化还原反应中,本身被还原 |
| D、氧化还原反应的实质是化合价的升降 |
下列说法正确的是( )
| A、H、D、T属于同位素,H2、D2、T2属于同素异形体 |
| B、氯水、氨水、王水是混合物,铁粉、漂白粉是纯净物 |
| C、HCl、NH3、BaSO4是电解质,CO2、Cl2、C2H5OH是非电解质 |
| D、风能、生物质能是可再生能源,煤、石油、天然气是不可再生能源 |
下列有关碳酸钠和碳酸氢钠的说法,不正确的是( )
| A、常温下在水中的溶解度:碳酸钠>碳酸氢钠 |
| B、热稳定性:碳酸钠<碳酸氢钠 |
| C、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 |
| D、等物质的量的碳酸和碳酸氢钠分别与足量的盐酸反应,两者产生二氧化碳一样多,但消耗的盐酸不一样多 |
下列关于硅的说法不正确的是( )
| A、硅是非金属元素,它的单质是灰黑色有金属光泽的固体 |
| B、硅的导电性能介于金属和绝缘体之间,是良好的半导体材料 |
| C、加热到一定温度时,硅能与氢气、氧气等非金属反应 |
| D、硅的化学性质不活泼,常温下不与任何物质起反应 |
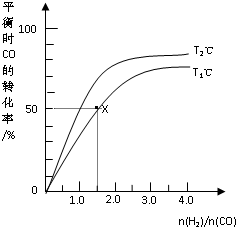 在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )
在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )| A、T1<T2 | ||
| B、T1℃时该反应的平衡常数为4.0 L2?mol-2 | ||
C、同一温度下,
| ||
D、相同条件下
|
下列说法正确的是( )
| A、反应:2CO(g)+2NO(g)?N2(g)+2CO2(g)在温度为298K时能自发进行,则它的△H>0,△S>0 |
| B、镀锌铁破损后会加快铁的腐蚀 |
| C、为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 |
| D、反应:2A(g)?B(g)+2C(g),增大压强反应速率加快,A的转化率减小 |
下列物质间的反应肯定无明显实验现象的是( )
| A、新鲜的玫瑰花放置于盛有干燥的Cl2的集气瓶中 |
| B、少量CO2通入浓的BaCl2溶液中 |
| C、将新制的氯水逐滴滴入含有酚酞的烧碱溶液中 |
| D、未经打磨的铝片加入浓NaOH溶液中一段时间 |