题目内容
下列有关碳酸钠和碳酸氢钠的说法,不正确的是( )
| A、常温下在水中的溶解度:碳酸钠>碳酸氢钠 |
| B、热稳定性:碳酸钠<碳酸氢钠 |
| C、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 |
| D、等物质的量的碳酸和碳酸氢钠分别与足量的盐酸反应,两者产生二氧化碳一样多,但消耗的盐酸不一样多 |
考点:钠的重要化合物
专题:元素及其化合物
分析:A.相同条件下碳酸钠较碳酸氢钠易溶;
B.NaHCO3不稳定,加热易分解;
C.利用n=
,可计算物质的量,因酸足量,利用Na2CO3~CO2,NaHCO3~CO2来分析;
D.结合反应的方程式分析.
B.NaHCO3不稳定,加热易分解;
C.利用n=
| m |
| M |
D.结合反应的方程式分析.
解答:
解;A.相同温度下相同的溶剂时,Na2CO3较NaHCO3易溶,在饱和碳酸钠溶液中通入二氧化碳,溶液变浑浊,可证明,故A正确;
B.加热时发生2NaHCO3
Na2CO3+CO2↑+H2O,而碳酸钠加热不分解,故B错误;
C.设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、
mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol、
mol,故C正确;
D.与盐酸分别发生:Na2CO3+2HCl=2NaCl+CO2↑+H2O、NaHCO3+HCl=NaCl+CO2↑+H2O,则物质的量相同时,生成二氧化碳体积相同,但消耗的盐酸不一样多,故D正确.
故选B.
B.加热时发生2NaHCO3
| ||
C.设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、
| 106 |
| 84 |
| 106 |
| 84 |
D.与盐酸分别发生:Na2CO3+2HCl=2NaCl+CO2↑+H2O、NaHCO3+HCl=NaCl+CO2↑+H2O,则物质的量相同时,生成二氧化碳体积相同,但消耗的盐酸不一样多,故D正确.
故选B.
点评:本题考查Na2CO3和NaHCO3性质的异同,题目难度不大,注意相同条件下,难溶性碳酸盐溶解度小于相应的碳酸氢盐,可溶性碳酸盐的溶解度大于相应的碳酸氢盐,为易错点.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
钢化玻璃具有高强度、抗震裂的性能,它适合用于制作( )
| A、太阳能电池 | B、高压输电线 |
| C、汽车挡风窗 | D、磁性合金 |
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液等五项操作.不正确的操作顺序是( )
| A、⑤④②①③ |
| B、④①②⑤③ |
| C、②⑤④①③ |
| D、⑤②④①③ |
下列装置中(杯中均盛海水)铁腐蚀最快的是( )
A、 |
B、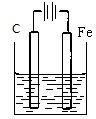 |
C、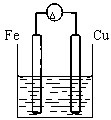 |
D、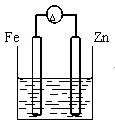 |
下列叙述正确的是( )
| A、非金属原子间以共价键结合的物质都是共价化合物 |
| B、制催化剂的材料和制耐高温、耐腐蚀的合金材料可在过渡元素中寻找 |
| C、1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 |
| D、铷的熔点比钠高,其硫酸盐易溶于水 |
下列变化中不可能通过实验直接一步完成的是( )
| A、Al→Al[(OH)4]- |
| B、Cu→CuSO4 |
| C、Fe(OH)2→Fe(OH)3 |
| D、NH3→HNO3 |
agCO2中含有b个分子,则阿伏加德罗常数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法中错误的是( )
| A、CO燃烧是放热反应 |
| B、浓硫酸在常温下能够使铁、铝等金属钝化 |
| C、CaO与H2O反应是吸热反应 |
| D、Na与NaCl在灼烧时火焰颜色相同 |