题目内容
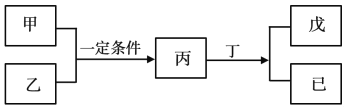
【题目】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________。人一旦吸入b气体后,就易引起中毒,是因为__________而中毒。
(3)c是双核单质,写出其电子式____________。c分子中所含共价键的类型为_______(填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________。
(4)d是四核化合物,其结构式为______________;d分子内所含共价键有________个σ键,________个π键;σ键与π键的强度大小关系为σ___π(填“>”、“<”或“=”),原因是:__________。
【答案】1s22s22p63s23p2 CO CO一旦被吸入肺里后,会与血液中的血红蛋白结合,使血红蛋白丧失输送氧气的能力 ![]() 非极性键 N2分子中的共价叁键键能很大,共价键很牢固 H—C≡C—H 3 2 > 形成σ键的原子轨道的重叠程度比π键的重叠程度大,形成的共价键强
非极性键 N2分子中的共价叁键键能很大,共价键很牢固 H—C≡C—H 3 2 > 形成σ键的原子轨道的重叠程度比π键的重叠程度大,形成的共价键强
【解析】
从a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子入手,并结合题目分析,a是Si;b是CO;c是N2;d是C2H2;
(1)a是Si,根据构造原理知,Si原子的电子排布式为1s22s22p63s23p2;
(2)b是两个原子的化合物,根据其物理性质:无色无味气体,推断b为CO,CO一旦进入肺里,会与血液中的血红蛋白结合而使血红蛋白丧失输送氧气的能力,使人中毒;
(3)c是双原子单质,每个原子有7个电子,故c为N2,N2分子的结构式为N≡N,为非极性键,N2分子中的共价叁键键能很大,所以N2分子很稳定,其电子式为:![]() ;
;
(4)d是四核化合物,即4个原子共有14个电子,d为C2H2,C2H2的结构式为H—C≡C—H,有两个H—C σ键,一个C—C σ键,两个π键。形成σ键的原子轨道的重叠程度比π键的重叠程度大,故形成的共价键强。