题目内容
【题目】下列仪器有“0”刻度线且“0”刻度线位置正确的是 ( )
A. 温度计的中部 B. 托盘天平刻度尺的中间
C. 量筒的下端 D. 容量瓶的上端
【答案】A
【解析】A.温度计0刻度在温度计的中间部分,故A正确;B.托盘天平的0刻度在刻度尺的左端,故B错误;C.量筒没有0刻度,量筒用于粗略量取液体体积,故C错误;D.容量瓶没有0刻度,只有一个刻度线,故D错误;故选A。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】如图所示,室温下,甲、乙两个容积相等的烧瓶中分别装满了两种气体(同温、同压)成份见下表,打开止水夹K,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是
编号 | ① | ② | ③ |
甲中气体 | H2 | NH3 | NO |
乙中气体 | Cl2 | HCl | O2 |
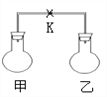
A. ②③① B. ③①② C. ③②① D. ①②③
【题目】某研究性学习小组通过下列反应原理制备SO2并进行性质探究。反应原理为:Na2SO3(固)+H2SO4(浓)= Na2SO4 + SO2↑+ H2O
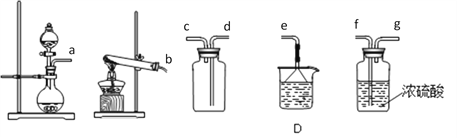
(1)根据上述原理制备并收集干燥SO2的实验装置连接顺序为________________。(填接头序号)
(2)D中盛装的试剂为_________________。
(3)甲同学用注射器吸取纯净的SO2并结合装置G进行SO2的性质实验,若X是Na2S溶液,其目的是检验SO2的_____________,可观察到的现象_________ 。
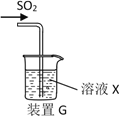
(4)实验1:乙同学将溶液X换为浓度均为0.1mol/L Fe(NO3)3和BaCl2的混合溶液(已经除去溶解氧),通入少量SO2后观察到烧杯产生白色沉淀,乙同学认为白色沉淀为BaSO4,为探究白色沉淀的成因,他继续进行如下实验验证:(已知:0.1mol/L Fe(NO3) 3的pH=2)
实验 | 操作 | 现象 | 结论和解释 |
2 | 将SO2通入0.1mol/L ____和BaCl2混合液 | 产生白色沉淀 | Fe3+能氧化H2SO3 |
3 | 将SO2通入_______ 和 BaCl2混合液 | 产生白色沉淀 | 酸性条件NO3-能将H2SO3氧化为SO42- |