题目内容
【题目】下列各图与表述一致的是
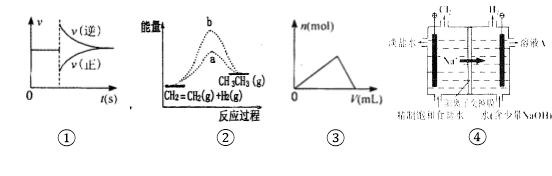
A.图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化
B.图②b曲线表示反应CH2=CH2(g)+H2(g)→CH3-CH3(g)ΔH <0,使用催化剂时,反应过程中的能量变化
C.曲线图③可以表示向一定量的氢氧化钠溶液中滴加一定浓度氯化铝溶液时产生沉淀的物质的量变化
D.图④电解饱和食盐水的装置中阴极的电极反应式为:2H++ 2e- = H2↑
【答案】D
【解析】
试题分析:A、当其他条件不变时,升高温度,正逆反应速率均加快;降低温度,正逆反应速率均减慢;与图像不符,错误;B、图②中a曲线表示反应CH2=CH2(g)+H2(g)→CH3-CH3(g)ΔH <0,使用催化剂时,反应过程中的能量变化,正确;C、向一定量的氢氧化钠溶液中滴加一定浓度氯化铝溶液时,一开始氢氧化钠溶液过量,无氢氧化铝沉淀生成,与图像不符,错误;D、图④电解饱和食盐水的装置中阴极的电极反应式为:2H++ 2e- = H2↑,正确。

练习册系列答案
相关题目
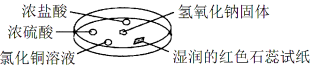
【题目】如图利用培养皿探究氨气的性质,实验时向NaOH固体上滴几滴浓氨水,立即用另一培养皿扣在上面。下表中对实验现象的描述及所做的解释均正确的是
选项 | 实 验 现 象 | 解 释 |
A | 浓盐酸附近产生白烟 | NH3与HCl反应生成了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化铜溶液变白色浑浊 | 白色浑浊的成分是Cu(OH)2 |
D | 湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |