题目内容
【题目】在隔绝空气的情况下,9.2 g铜、镁混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到标准状况下4.48 LNO气体。向反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为
A.19.4 gB.18.6 gC.20 gD.24 g
【答案】A
【解析】
硝酸与金属反应生成一氧化氮:HNO3~NO氮元素化合价降低了3价,生成1mol NO得到3mole-,标况下4.48L NO的物质的量为:n(NO)=![]() =0.2mol,得到电子的物质的量为:n(e-)=0.2mol×3=0.6mol,根据金属的转化关系:M~Mn+~M(OH)n和电子守恒可知,金属失去电子的物质的量等于硝酸中N原子得到电子的物质的量,也等于生成沉淀时结合OH-的物质的量,即:n(OH-)=n(e-)=0.6mol ,则生成沉淀的最大质量为:金属质量+净增OH-的质量=9.2g+0.6mol×17g/mol=19.4g,故A正确。
=0.2mol,得到电子的物质的量为:n(e-)=0.2mol×3=0.6mol,根据金属的转化关系:M~Mn+~M(OH)n和电子守恒可知,金属失去电子的物质的量等于硝酸中N原子得到电子的物质的量,也等于生成沉淀时结合OH-的物质的量,即:n(OH-)=n(e-)=0.6mol ,则生成沉淀的最大质量为:金属质量+净增OH-的质量=9.2g+0.6mol×17g/mol=19.4g,故A正确。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
【题目】某同学利用下图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )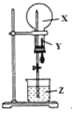
X气体 | Y试剂 | Z试剂 | |
A. | NO2 | H2O | H2O |
B. | CO2 | H2O | H2O |
C. | HCl | 饱和食盐水 | 水 |
D. | NO2 和O2 | H2O | H2O |
A.AB.BC.CD.D