题目内容
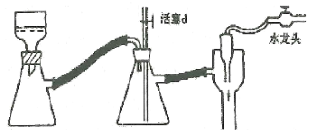
【题目】海洋植物如海带、海藻中含有丰富的碘元素,且所含碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图所示:

(1)指出制取碘的过程中有关实验操作的名称:①__________,②__________。
(2)操作②中可供选择的有机试剂是_________(填序号)。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(3)现需做使海藻灰中的碘离子转化为有机溶液中的碘单质的实验,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、药品,尚缺少的玻璃仪器是__________、___________。
(4)要从碘的苯溶液中提取碘和回收苯,还需要经过蒸馏操作。进行蒸馏操作时,需使用水浴加热,目的是__________,最后晶态碘在________中聚集。
【答案】过滤 萃取和分液 B 普通漏斗 分液漏斗 使蒸馏烧瓶均匀受热,控制温度不过高 蒸馏烧瓶
【解析】
(1)从海藻中提取碘的流程为灼烧、浸泡、过滤、氧化、萃取分液、蒸馏;
(2)操作②为萃取,萃取剂的选择需符合与氯水互不相溶,碘的溶解度较大;
(3)使海藻灰中的碘离子转化为有机溶液中的碘单质的实验,需要的操作有浸泡、过滤、氧化、萃取分液,以此分析所需实验仪器;
(4)进行蒸馏操作时,需使用水浴加热,目的是使蒸馏烧瓶均匀受热,控制温度不过高,防止苯蒸发,最后晶态碘在蒸馏烧瓶中凝华聚集。
(1) 从海藻中提取碘的流程为灼烧、浸泡、过滤、氧化、萃取、蒸馏,由图可知操作①是过滤,操作②是萃取和分液,
故答案为:过滤;萃取和分液;
(2) 操作②为萃取,萃取剂的选择需符合与氯水互不相溶,碘的溶解度较大,由于酒精、乙酸和甘油都与水互溶,故不能用作提取碘的萃取剂,
故答案选:B。
(3)为使海藻灰中的碘离子转化为有机溶液中的碘单质,需经过溶解、过滤、氧化、萃取和分液这几个步骤。在过滤时缺少普通漏斗,在进行萃取和分液时缺少分液漏斗,
故答案为:普通漏斗;分液漏斗;
(4)苯的沸点为80.1℃。使用水浴加热的目的是使蒸馏烧瓶均匀受热,控制温度不过高(水浴加热时的温度不会超过100℃)。最后晶态碘在蒸馏烧瓶中聚集,
故答案为:使蒸馏烧瓶均匀受热,控制温度不过高;蒸馏烧瓶。

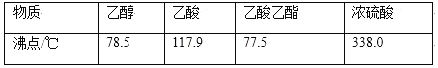
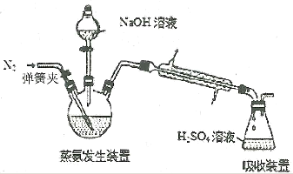
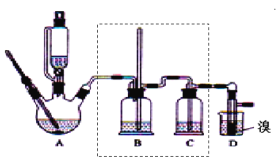
【题目】实验室制备1,2—二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2—二溴乙烷,装置如图所示。有关数据列表如表所示。回答下列问题:
乙醇 | 1,2—二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是__。
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置A中除了浓硫酸和乙醇外,还应加入__,其目的是__。装置A中生成副产物乙醚的化学反应方程式为__。
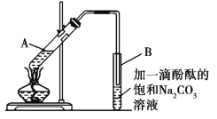
(3)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,为了验证SO2的存在并除去SO2对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放___。
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液 d.品红和酸性KMnO4
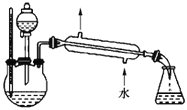
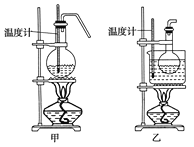
(4)甲、乙两装置均可用作实验室由无水乙醇制取乙烯,乙图采用甘油浴加热(甘油沸点290℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有无水乙醇和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。甲、乙两装置相比较,乙装置有哪些优点__,写出该实验中由无水乙醇制取乙烯的化学方程式___。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置后,产物应在__层;若产物中有少量副产物乙醚。可用__的方法除去。