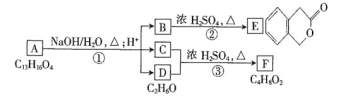
题目内容
【题目】资料在线:查阅资料可知如表所示数据:
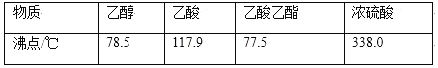
[实验步骤]
某学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4配制浓硫酸、乙醇和乙酸的混合溶液;
②按如图所示连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10 min;
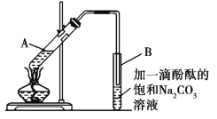
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥。
请根据题目要求回答下列问题:
(1)步骤①配制该混合溶液的主要操作步骤为___;写出制取乙酸乙酯的化学方程式:___。
(2)步骤②中需要小火均匀加热,其主要理由是________。
(3)指出步骤③所观察到的现象:________;
分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为____(填字母)。
A.P2O5 B.无水Na2SO4
C.碱石灰 D.NaOH固体
(4)某化学课外小组设计了如图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有______。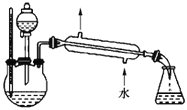
【答案】在一支30 mL的大试管(A)中注入4 mL乙醇,缓慢加入1 mL的浓硫酸,边加边振荡试管,待冷却至室温时,再加入4 mL乙酸并摇匀 CH3COOH+C2H5OH![]() CH3COOC2H5+H2O 一方面,用大火加热,反应物容易随生成物(乙酸乙酯)一起蒸出来,导致原料的大量损失;另一方面,温度太高,可能发生其他副反应 试管B中的液体分成上下两层,上层油状液体无色(可以闻到水果香味),下层液体显(浅)红色,振荡后下层液体的红色变浅 B ①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙酯
CH3COOC2H5+H2O 一方面,用大火加热,反应物容易随生成物(乙酸乙酯)一起蒸出来,导致原料的大量损失;另一方面,温度太高,可能发生其他副反应 试管B中的液体分成上下两层,上层油状液体无色(可以闻到水果香味),下层液体显(浅)红色,振荡后下层液体的红色变浅 B ①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙酯
【解析】
(1)配制乙醇、浓硫酸、乙酸混合液时,各试剂加入试管的顺序依次为:CH3CH2OH浓H2SO4CH3COOH;乙酸与乙醇反应的方程式为:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(2)若用大火加热,反应物容易随生成物(乙酸乙酯)一起蒸出来,导致原料的大量损失;另一个方面,温度太高,可能发生其他副反应;
(3)步骤③中的主要现象是:试管B中的液体分成上下两层,上层油状液体无色(可以闻到水果香味),下层液体(浅)红色,振荡后下层液体的红色变浅;
(4)①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了水冷凝装置,有利于收集产物乙酸乙酯。
(1)配制乙醇、浓硫酸、乙酸混合液时,各试剂加入试管的顺序依次为:CH3CH2OH浓H2SO4CH3COOH,将浓H2SO4加入乙醇中,边加边振荡是为了防止混合时产生热量导致液体飞溅造成事故;将乙醇与浓H2SO4的混合液冷却后再与乙酸混合,是为了防止乙酸的挥发造成原料的损失。在加热时试管中所盛溶液不能超过试管容积的1/3。因为试管容积为30mL,那么所盛溶液不超过10mL,按体积比1∶4∶4的比例配浓H2SO4、乙酸和乙醇的混合溶液,由此可知,对应的浓硫酸、乙酸和乙醇的体积为1mL、4mL、4mL。配制混合溶液的主要操作步骤可叙述为:在一支30mL的大试管(A)中注入4mL乙醇,缓慢加入1mL的浓硫酸,边加边振荡试管,待冷却至室温时,再加入4mL乙酸并摇匀,其反应的化学方程式为CH3COOH+C2H5OH![]() CH3COOC2H5+H2O;故答案为在一支30mL的大试管(A)中注入4mL乙醇,缓慢加入1mL的浓硫酸,边加边振荡试管,待冷却至室温时,再加入4mL乙酸并摇匀;CH3COOH+C2H5OH
CH3COOC2H5+H2O;故答案为在一支30mL的大试管(A)中注入4mL乙醇,缓慢加入1mL的浓硫酸,边加边振荡试管,待冷却至室温时,再加入4mL乙酸并摇匀;CH3COOH+C2H5OH![]() CH3COOC2H5+H2O。
CH3COOC2H5+H2O。
(2)由题中给出的各物质的主要物理性质,根据各物质的沸点数据可知,乙酸(117.9℃)、乙醇(78.0℃)的沸点都比较低,且与乙酸乙酯的沸点(77.5℃)比较接近,若用大火加热,反应物容易随生成物(乙酸乙酯)一起蒸出来,导致原料的大量损失;另一个方面,温度太高,可能发生其他副反应,故答案为一方面,用大火加热,反应物容易随生成物(乙酸乙酯)一起蒸出来,导致原料的大量损失;另一方面,温度太高,可能发生其他副反应。
(3)在步骤③中的主要现象是:试管B中的液体分成上下两层,上层油状液体无色(可以闻到水果香味),下层液体(浅)红色,振荡后下层液体的红色变浅。分离出来的是粗产品乙酸乙酯层,乙酸乙酯粗产品的提纯方法步骤为:①向粗产品中加入碳酸钠粉末(目的是除去粗产品中的乙酸);②向其中加入饱和食盐水与饱和氯化钙溶液,振荡、静置、分液(目的是除去粗产品中的乙醇);③向其中加入无水硫酸钠(目的是除去粗产品中的水);④最后将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏,弃去低沸点馏分,收集温度在76-78℃之间的馏分即得纯的乙酸乙酯,故选B项,故答案为试管B中的液体分成上下两层,上层油状液体无色(可以闻到水果香味),下层液体显(浅)红色,振荡后下层液体的红色变浅;B。
(4)对比两个实验装置图结合乙酸乙酯制备过程中的各种条件控制,可以看出后者的三个突出的优点:①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了水冷凝装置,有利于收集产物乙酸乙酯,故答案为①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的产生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙酯。

【题目】用中和滴定法测定某烧碱样品的纯度,假设烧碱样品中的杂质(可溶于水)与酸不反应,试根 据实验回答下列问题:
(1)将准确称取的 4.3 g 烧碱样品配成 250 mL 待测液,需要的主要仪器除烧杯、玻璃棒外,还必须用到的仪器有______、______。
(2)取10.00 mL 待测液,用图中____(填“甲”或“乙”)量取。
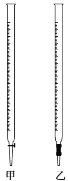
(3)用 0.2010 mol·L-1 的标准盐酸滴定待测烧碱溶液(用酚酞做指示剂),滴定时左手旋转 酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶中溶液颜色的变化,直到_____________,即达到滴定终点。
(4)根据表中数据,可计算出烧碱的纯度为____(用百分数表示,结果保留小数点后一位小数)。
滴定次数 | 待测液 体积/mL | 标准盐酸体积/mL | |
滴定前读数/mL | 滴定后读数/mL | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
(5)排去碱式滴定管中的气泡应采用操作______(填“甲”“乙”或“丙”),然后轻轻挤压玻璃球使尖嘴部分充满碱液。
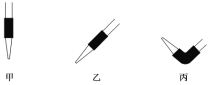
(6)在该滴定实验中,下列操作(其他操作正确)会造成测定结果偏高的是_____(填序号)。
A 滴定终点读数时俯视读数
B 酸式滴定管水洗后未用标准盐酸润洗
C 锥形瓶水洗后未干燥
D 锥形瓶用蒸馏水洗后又用待测液润洗
E 滴定到指示剂刚变色,摇动锥形瓶后颜色恢复,没再继续滴定
F 酸式滴定管尖嘴部分有气泡,滴定后气泡消失
【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为:
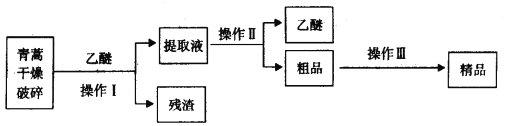
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是______。
(2)操作I需要的玻璃仪器主要有:烧杯、______。
(3)在操作Ⅱ的蒸馏操作中,仪器选择及安装都正确的是______(填标号)。
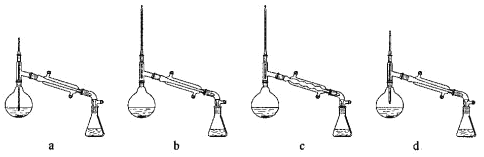
(4)操作Ⅲ的主要过程可能是______(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(5)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
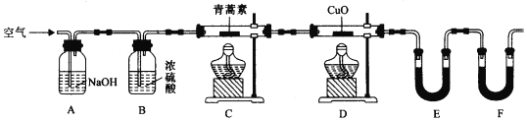
①装置E中盛放的物质是______,装置F中盛放的物质是______。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______。
③用合理改进后的装置进行试验,称得:
装置 | 实验前 | 实验后 |
E |
|
|
F |
|
|
则测得青蒿素的最简式是______。
(6)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与______(填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖