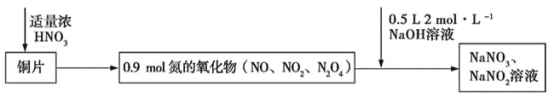
题目内容
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
(1)第一份加入![]() 溶液有沉淀产生
溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体![]()
(3)第三份加足量![]() 溶液后,得干燥沉淀
溶液后,得干燥沉淀![]() ,经足量盐酸洗涤、干燥后,沉淀质量为
,经足量盐酸洗涤、干燥后,沉淀质量为![]() 。根据上述实验,确定一定存在的离子是______;可能存在的离子是______;一定不存在的离子是______。
。根据上述实验,确定一定存在的离子是______;可能存在的离子是______;一定不存在的离子是______。
【答案】![]() 、
、![]() 、
、![]() 、
、![]()
![]()
![]() 、
、![]()
【解析】
(1)第一份加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol,气体为氨气,溶液中一定含有NH4+,并且物质的量为0.04mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g,则2.33g沉淀为硫酸钡,6.27g沉淀为硫酸钡和碳酸钡的混合物;再根据电荷守恒,判断是否存在钾离子,据此进行解答。
(1)第一份加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol,气体为氨气,溶液中一定含有NH4+,并且物质的量为0.04mol;
(3)2.33g沉淀为硫酸钡,其物质的量=![]() =0.01mol,碳酸钡物质的量=
=0.01mol,碳酸钡物质的量=![]() =0.02mol,则溶液中一定存在CO32-、SO42-,一定不存在Mg2+、Ba2+,再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;c(-)=2c(CO32-)+2c(SO42-)=0.06mol,正电荷总物质的量小于负电荷,故原溶液中一定有K+,可能存在Cl-,即溶液中一定存在NH4+、K+、CO32-、SO42-,可能存在Cl-,一定不存在Ba2+、Mg2+,故答案为:NH4+、K+、CO32-、SO42-;Cl-;Ba2+、Mg2+。
=0.02mol,则溶液中一定存在CO32-、SO42-,一定不存在Mg2+、Ba2+,再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;c(-)=2c(CO32-)+2c(SO42-)=0.06mol,正电荷总物质的量小于负电荷,故原溶液中一定有K+,可能存在Cl-,即溶液中一定存在NH4+、K+、CO32-、SO42-,可能存在Cl-,一定不存在Ba2+、Mg2+,故答案为:NH4+、K+、CO32-、SO42-;Cl-;Ba2+、Mg2+。

【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为:
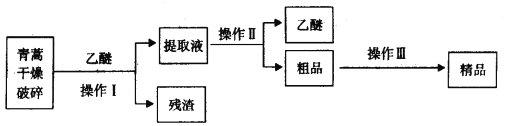
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是______。
(2)操作I需要的玻璃仪器主要有:烧杯、______。
(3)在操作Ⅱ的蒸馏操作中,仪器选择及安装都正确的是______(填标号)。
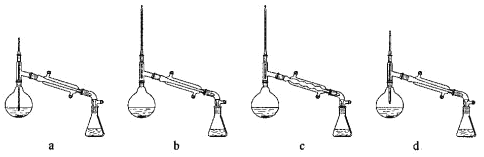
(4)操作Ⅲ的主要过程可能是______(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(5)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
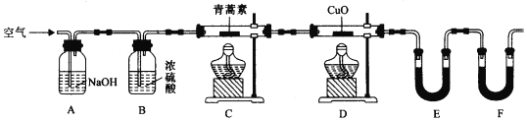
①装置E中盛放的物质是______,装置F中盛放的物质是______。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______。
③用合理改进后的装置进行试验,称得:
装置 | 实验前 | 实验后 |
E |
|
|
F |
|
|
则测得青蒿素的最简式是______。
(6)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与______(填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
【题目】在下图装置中,烧瓶中充满干燥气体a,将胶头滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。a和b分别可以是
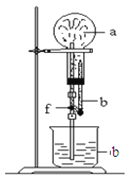
干燥气体a | 液体b | |
A | NO2 | 水 |
B | C12 | 饱和食盐水 |
C | NH3 | 水 |
D | CO2 | 4 mol·L—1NaOH溶液 |
A.AB.BC.CD.D