题目内容
【题目】(1)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.
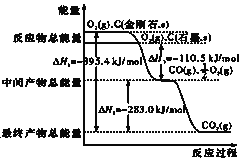
a.在通常状况下,金刚石和石墨相比较_____,(填”金刚石”或”石墨”)更稳定,石墨的燃烧热为_____.
b.12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为_____.
(2)已知:N2、O2分子中化学键的键能分别是946kJmol﹣1、497kJmol﹣1.N2(g)+O2(g)═2NO(g)△H=+180.0kJ·mol﹣1.NO分子中化学键的键能为_____kJ·mol﹣1.
(3)综合上述有关信息,请写出用CO除去NO的热化学方程式:_____.
【答案】石墨 ﹣393.5kJmol﹣1 252.0 kJ 631.5 2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=﹣746.0kJmol﹣1
【解析】
(1)(a)图象分析金刚石能量高于石墨,能量越低越稳定,所以说明石墨稳定,图象分析1mol石墨完全燃烧生成1mol二氧化碳放出的热量为393.5kJ,则石墨的燃烧热为△H=﹣393.5kJmol﹣1;
故答案为:石墨;﹣393.5kJmol﹣1;
(b)12g石墨物质的量为1mol,在一定量空气中燃烧,依据元素守恒,若生成二氧化碳质量为44g,若生成一氧化碳质量为28g,生成气体36g,28g<36g<44g,判断生成的气体为一氧化碳和二氧化碳气体,设一氧化碳物质的量为x,二氧化碳物质的量为(1﹣x)mol,28x+44(1﹣x)=36g,x=0.5mol,二氧化碳物质的量为0.5mol;依据图象分析,C(石墨,s)+O2(g)═CO2(g)△H=﹣393.5 kJmol﹣1 ;C(石墨,s)![]() O2(g)═CO(g)△H=﹣110.5 kJmol﹣1
O2(g)═CO(g)△H=﹣110.5 kJmol﹣1
生成二氧化碳和一氧化碳混合气体放出热量=393.5 kJmol﹣1 ×0.5mol+110.5 kJmol﹣1 ×0.5mol=252kJ;12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为252.0kJ;
故答案为:252.0 kJ;
(2)△H=反应物键能和﹣生成物键能和,946kJ/mol+497kJ/mol﹣2Q(N﹣O)=180.0kJ/mol,Q(N﹣O)=631.5kJ/mol,故答案为:631.5;
(3)已知①C(石墨,s)+O2(g)=CO2(g)△H=﹣393.5 kJmol﹣1;
②C(石墨,s)![]() O2(g)=CO(g)△H=﹣110.5 kJmol﹣1;
O2(g)=CO(g)△H=﹣110.5 kJmol﹣1;
③N2(g)+O2(g)=2NO(g)△H=+180kJmol﹣1;
由盖斯定律:方程式①×2﹣②×2﹣③得 2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=﹣746.0kJmol﹣1;
故答案为:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=﹣746.0kJmol﹣1;