��Ŀ����
����Ŀ�������£���0.1000 mol��L��1�������20.00 mL 0.100 0mol��L��1��ijһԪ��MOH��Һ�У���Һ��pH�������������仯��������ͼ��ʾ�������й�˵������ȷ����( )

A.��һԪ��ĵ��뷽��ʽΪMOH �� M+��OH��
B.a��b��c�����У�b��ˮ�ĵ���̶����
C.�����£�MOH�ĵ��볣��Kb��1��10��5 mol��L��1
D.b�㣺c (M+)��c (Cl��)
���𰸡�A
��������
A. ����ͼ��0.100 0mol��L��1��һԪ��MOH��pH=11����c(OH-)=0.001mol/L,��һԪ��Ϊ�������뷽��ʽΪMOHM+��OH�����������⣬A��ȷ��
B. ����ͼ��aΪ���������Һ��b����Һ�����ԣ�cΪ���������Һ���ᡢ���ˮ�ĵ������������ã��������У�b��ˮ�ĵ���̶���������ⲻ����B����
C. �����£�MOH�ĵ��볣��Kb��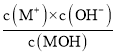 =
=![]() =1��10��5 mol��L��1�������ⲻ����C����
=1��10��5 mol��L��1�������ⲻ����C����
D. b����Һ�����ԣ���c(H+)��c(OH-)��������Һ�ʵ����ԣ�c (M+)+ c(H+)��c (Cl��)+c(OH-)���õ�c (M+)��c (Cl��)�������ⲻ����D����
��ΪA��

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ