题目内容
下列说法中(NA代表阿伏加德罗常数),不正确的是( )
| A、常温常压下,18g H2O含有的原子总数为3NA |
| B、标准状况下,2.24L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| C、常温下,2.3g Na完全与O2反应失去的电子数为0.1NA |
| D、在密闭容器中加入1.5mol H2和0.5mol N2,充分反应后可得到NH3分子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.18g水的物质的量为1mol,1mol水中含有3mol原子;
B.标况下2.24L一氧化碳和二氧化碳的混合气体的物质的量为0.1mol,含有0.1molC;
C.钠为1价金属,2.3g钠的物质的量为0.1mol,完全反应0.1mol钠失去0.1mol电子;
D.氮气与氢气的反应为可逆反应,反应物不可能完全转化成生成物.
B.标况下2.24L一氧化碳和二氧化碳的混合气体的物质的量为0.1mol,含有0.1molC;
C.钠为1价金属,2.3g钠的物质的量为0.1mol,完全反应0.1mol钠失去0.1mol电子;
D.氮气与氢气的反应为可逆反应,反应物不可能完全转化成生成物.
解答:
解:A.18g水的物质的量为1mol,1mol水中含有2nol氢原子、1mol氧原子,总共含有3mol原子,含有的原子总数为3NA,故A正确;
B.标准状况下,2.24L CO和CO2混合气体中含有气体的物质的量为0.1mol,0.1mol混合气体中含有0.1mol碳原子,含有碳原子数目为0.1NA,故B正确;
C.2.3g钠的物质的量为0.1mol,0.1mol钠完全反应失去0.1mol电子,失去的电子数为0.1NA,故C正确;
D.在密闭容器中加入1.5mol H2和0.5mol N2,合成氨为可逆反应,反应生成的氨气小于1mol,分反应后可得到NH3分子数小于NA,故D错误;
故选D.
B.标准状况下,2.24L CO和CO2混合气体中含有气体的物质的量为0.1mol,0.1mol混合气体中含有0.1mol碳原子,含有碳原子数目为0.1NA,故B正确;
C.2.3g钠的物质的量为0.1mol,0.1mol钠完全反应失去0.1mol电子,失去的电子数为0.1NA,故C正确;
D.在密闭容器中加入1.5mol H2和0.5mol N2,合成氨为可逆反应,反应生成的氨气小于1mol,分反应后可得到NH3分子数小于NA,故D错误;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意氮气与氢气的反应为可逆反应,反应物主链不可能为100%.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
常温下,通过测定气体的密度可以求出下列气体的摩尔质量,其中误差较大的是( )
| A、CO2 |
| B、H2 |
| C、NO2 |
| D、CH4 |
用下列方法来制备溶胶:①0.5mol/L BaCl2溶液和等体积2mol/L硫酸相混合并振荡;②把5、6滴饱和三氯化铁溶液滴加入20mL沸水中,边加边振荡;③将盐酸逐滴加入到饱和Na2SiO3溶液中,用力振荡.可行的是( )
| A、①② | B、①③ | C、②③ | D、①②③ |
下列反应的离子方程式表示正确的是( )
| A、向Fe(NO3)3溶液中加入过量的HI溶液:2NO3-+8H++6I-═3I2+2NO↑+4H2O |
| B、硫酸溶液中加入足量氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| C、亚硫酰氯(SOCl2)剧烈水解生成两种酸:SOCl2+2H2O═H2SO3+2H++2Cl- |
| D、将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中:CO2+SO2+4OH-═SO32-+CO32-+2H2O |
复合物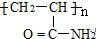 的单体是( )
的单体是( )
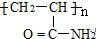 的单体是( )
的单体是( )A、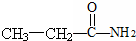 |
B、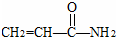 |
| C、CH2=CH2 |
D、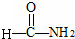 |
温下,某溶液中由水电离出来的c(OH-)=1.0×10-14mol?L-2,下列离子组中,可以在该溶液中大量共存的是( )
| A、Al3+、Fe3+、NO3-、I- |
| B、K+、Na+、Cl-、SO42- |
| C、Mg2+、Ca2+、CO32-、AlO2- |
| D、K+、NH4+、SO42-、HCO3- |
已知25℃时,Ksp(AgI)=8.5×10-17,Ksp(AgCl)=1.8×10-10,若在5mL含有KCl和KI均为0.01mol?L-1的溶液中,缓慢滴加8mL 0.01moL-1 AgNO3溶液,下列叙述正确的是( )
| A、混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | ||
| B、混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) | ||
| C、加入AgNO3溶液时首先生成AgCl沉淀 | ||
D、混合溶液中
|
一定条件下,X(g)+3Y(g)?2Z(g)达到平衡的标志是( )
| A、Z的分解速率和生成速率相等 |
| B、X、Y、Z的浓度比为1:3:2 |
| C、反应体系的总质量保持不变 |
| D、单位时间内生成n mol Z,同时生成n mol X |
 中学常见物质A、B、C、D、E、X,存在如图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在如图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )| A、若D为NaCl,且A可与C反应生成B,则E可能是CO2 |
| B、若D是一种强碱,则A、B、C均可与X反应生成D |
| C、若D是一种白色沉淀,在空气中最终变成红褐色,则A可能是铁 |
| D、若D是一种弱酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |