题目内容
一定条件下,X(g)+3Y(g)?2Z(g)达到平衡的标志是( )
| A、Z的分解速率和生成速率相等 |
| B、X、Y、Z的浓度比为1:3:2 |
| C、反应体系的总质量保持不变 |
| D、单位时间内生成n mol Z,同时生成n mol X |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A.Z的分解速率和生成速率相等,说明正逆反应速率相等,该反应达到平衡状态,故A正确;
B.平衡时A、B、C 的浓度之比可能为1:3:2,可能不是1:3:2,与反应物的起始物浓度、转化率有关,所以不能判断该反应是否达到平衡状态,故B错误;
C.反应中遵循质量守恒,无论何时反应体系的总质量保持不变,所以不能判断该反应是否达到平衡状态,故C错误;
D.单位时间内生成n mol Z,同时生成n mol X,正逆反应速率不相等,所以不能判断该反应是否达到平衡状态,故D错误;
故选A.
B.平衡时A、B、C 的浓度之比可能为1:3:2,可能不是1:3:2,与反应物的起始物浓度、转化率有关,所以不能判断该反应是否达到平衡状态,故B错误;
C.反应中遵循质量守恒,无论何时反应体系的总质量保持不变,所以不能判断该反应是否达到平衡状态,故C错误;
D.单位时间内生成n mol Z,同时生成n mol X,正逆反应速率不相等,所以不能判断该反应是否达到平衡状态,故D错误;
故选A.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
下列说法中(NA代表阿伏加德罗常数),不正确的是( )
| A、常温常压下,18g H2O含有的原子总数为3NA |
| B、标准状况下,2.24L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| C、常温下,2.3g Na完全与O2反应失去的电子数为0.1NA |
| D、在密闭容器中加入1.5mol H2和0.5mol N2,充分反应后可得到NH3分子数为NA |
将2.3g钠溶于100g水中,所得溶质的质量分数为( )
| A、2.25% |
| B、2.30% |
| C、3.91% |
| D、4.00% |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,48g O2和O3组成的混和气体中所含的氧原子数为3NA |
| B、2mol H2O中含有36NA个电子 |
| C、2L 0.1mol?L-1 H2SO4溶液中含有0.2NA个H+ |
| D、常温常压下,22.4L CH4中含有NA个CH4分子 |
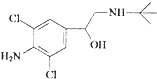 去年央视“315特别行动”又曝光了河南一些地方“瘦肉精”事件.“瘦肉精”对人体健康会产生危害.已知某中“瘦肉精”含有克伦特罗(Clenbuterol),其结构如图.下列有关克伦特罗的叙述,正确的是( )
去年央视“315特别行动”又曝光了河南一些地方“瘦肉精”事件.“瘦肉精”对人体健康会产生危害.已知某中“瘦肉精”含有克伦特罗(Clenbuterol),其结构如图.下列有关克伦特罗的叙述,正确的是( )| A、该物质的分子式为C12H16ON2Cl2 |
| B、该物质不能与盐酸反应 |
| C、该物质的核磁共氢振谱图中有9个吸收峰 |
| D、该物质能发生的类型有:加成反应、酯反应、消去反应、氧化反应等 |
下列实验中,溶液颜色有明显变化的是( )
| A、少量明矾溶液加入到过量NaOH溶液中 |
| B、往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C、少量Na2O2固体加入到过量NaHSO3溶液中 |
| D、往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液 |
下列分子式只能表示一种物质的是( )
| A、C3H7Cl |
| B、CH2Cl2 |
| C、C3H6O |
| D、C3H4O2 |
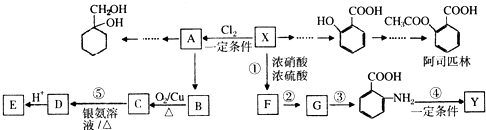
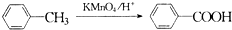
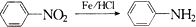 (苯胺,易被氧化)
(苯胺,易被氧化)