题目内容
2.某同学在实验室进行实验:将一定量蔗糖放入烧杯中,加入少量水搅拌均匀,再加适量 浓硫酸迅速搅拌,产生如下现象:①烧杯立即发热 ②片刻后蔗糖发黄变黑 ③稍后体积 迅速膨胀,产生刺激性气味的气体.下列对该实验的相关说法不正确的是( )| A. | 现象①-浓硫酸吸水放热 | |
| B. | 现象②-浓硫酸具有脱水性使蔗糖炭化 | |
| C. | 现象③-浓硫酸具有强氧化性,发生反应:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O | |
| D. | 若将③中气体通入澄清石灰水中,出现白色浑浊,可证明气体中存在CO2 |
分析 因浓硫酸具有吸水性,浓硫酸吸水稀释而放出大量的热,浓硫酸将蔗糖中的H和O以2:1的形式脱去,蔗糖变黑;浓硫酸具有强氧化性:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,产生有刺激性气味的气体,由此分析解答.
解答 解:A、浓硫酸具有吸水性,浓硫酸吸水稀释而放出大量的热,所以烧杯立即发热,故A正确;
B、浓硫酸将蔗糖中的H和O以2:1的形式脱去,蔗糖变黑,体现浓硫酸的脱水性,故B正确;
C、浓硫酸具有强氧化性:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,产生有刺激性气味的气体,故C正确;
D、能使澄清石灰水中,出现白色浑浊的气体有二氧化碳和二氧化硫,所以不一定是二氧化碳,故D错误;
故选D.
点评 本题主要考查了浓硫酸的强氧化性、三大特性,同时考查了氧化还原反应的有关知识,氧化还原反应的概念容易混淆,要注意区分.

练习册系列答案
相关题目
12.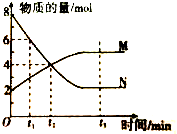 在一定温度下,容器内某一反应中的M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中的M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,容器内某一反应中的M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中的M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | t2时,正逆反应速率相等 | B. | t1时,N的浓度是M浓度的2倍 | ||
| C. | t3时,正反应速率大于逆斥速率 | D. | t3时,正反应速率等于逆反应速率 |
13.下列说法正确的是( )
| A. | 取碳酸钾固体进行焰色反应实验时,要透过蓝色钴玻璃观察火焰的颜色 | |
| B. | 漂白粉是纯净物,它的成分为次氯酸钙 | |
| C. | 实验室制备Cl2时,可用排烧碱溶液集气法收集 | |
| D. | 加碘食盐能使淀粉溶液变蓝 |
10.下列说法不正确的是( )
| A. | 盛有浓H2SO4 的烧杯在空气中敞口放置一段时间后,质量增加 | |
| B. | SO2 溶于水能导电,所以SO2 是电解质 | |
| C. | 标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内的氨水物质的量浓度为$\frac{1}{22.4}$ mol/L | |
| D. | 用蘸占有稀氨水的毛笔,在浸有酚酞溶液的滤纸上写出的字呈红色 |
17.下列物质不能由氯气与单质直接化合制得的是( )
| A. | HCl | B. | FeCl2 | C. | CuCl2 | D. | NaCl |
7.下列关于Na2O2的说法中,不正确的是( )
| A. | 浅黄色固体 | B. | 可用作供氧剂 | ||
| C. | 与H2O反应时,H2O作还原剂 | D. | 与H2O反应时,放出热量 |
11.由钠、镁、铝、铁四种金属中的两种组成的混合物12克,与足量盐酸反应生成氢气0.5克,则该混合物的组成可能是( )
| A. | 钠和镁 | B. | 钠和铝 | C. | 钠和铁 | D. | 镁和铝 |

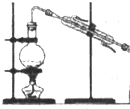
 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示.回答下列问题:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示.回答下列问题: