题目内容
【题目】某温度下,在体积可变的容器中发生反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(l),改变起始时加入各物质的量,在不同压强下达平衡时CH3OCH3(g)的物质的量如表所示,下列说法错误的是( )
CH3OCH3(g)+3H2O(l),改变起始时加入各物质的量,在不同压强下达平衡时CH3OCH3(g)的物质的量如表所示,下列说法错误的是( )
压强 | P1 | P2 | P3 | |
n/mol | ①2.0molCO2 6.0molH2 | 0.10mol | 0.04mol | 0.02mol |
②1.0molCO2 3.0molH2 | x 1 | y 1 | z 1 | |
③1.0molCH3OCH3 3.0molH2O | x 2 | y 2 | z 2 | |
A.P1>P2B.x 1=0.05
C.P2条件下,③中CH3OCH3平衡转化率为96%D.若该反应可自发进行,则高温更有利
【答案】D
【解析】
相同温度和压强下,只要使各物质初始浓度对应成比例即可建立等效平衡,则在相同温度和压强下,①②③互为等效平衡。
A、根据①以及反应是体积减小的反应,压强越大,会正向移动,P1时CH3OCH3(g)的物质的量为0.10mol,P2时CH3OCH3(g)的物质的量为0.04mol,因此P1>P2,故A正确,不符合题意;
B、①②处于平衡状态时是等效的,②的起始量是①的一半,则平衡时x 1=0.05,故B正确,不符合题意;
C、P2条件下,①③是完全等效的,平衡时CH3OCH3(g)的物质的量为0.04mol,转化了0.96mol,平衡转化率为96%,故C正确,不符合题意;
D、该反应是ΔS < 0,若该反应可自发进行,则低温更有利,故D错误,符合题意;
综上所述,答案为D。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案【题目】雾霾天气严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染。
请回答下列问题:
(1)汽车尾气中NOx和CO的生成:已知汽缸中生成NO的反应为:N2(g)+O2(g)![]() 2NO(g)—Q。恒温、恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。
2NO(g)—Q。恒温、恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是____。
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.N2、O2、NO的物质的量之比为1∶1∶2
D.氧气的转化率不再变化
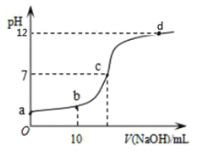
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究性小组在实验室以Ag—ZSM—5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为___,在![]() =1的条件下,为更好的除去NOx,应控制的最佳温度在___K左右。
=1的条件下,为更好的除去NOx,应控制的最佳温度在___K左右。

(3)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
物质 温度(℃) | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式:___。
②若T1<T2,则该反应的Q__0(填“>”“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为___。
【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以纯铜屑为原料制取的流程如下:
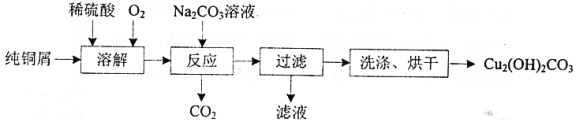
(1)“溶解”步骤反应的离子方程式为_______.温度宜控制在50℃左右,若高于50℃,溶液中O2溶解量减少、Cu的转化率降低,若低于50℃ ,_____
(2)“反应”步骤生成Cu2(OH)2CO3的化学方程式为_________。反应后溶液中铜元素残留量受pH和反应时间的影响如图所示:
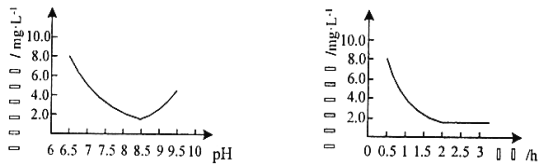
判断反应的最佳条件: pH为___、反应时间为____h。
(3)检验Cu2(OH)2CO3洗涤是否完全的方法是____________________
(4) Cu2(OH)2CO3也可以表示为CuCO3·Cu(OH)2。 查阅文献,上述反应条件下还可能生成少量CuCO3·Cu(OH)2。为测定产品的纯度[产品中Cu2(OH)2CO3的质量分数],取10.97g干燥样品,400℃左右加热,测得固体质量随时间变化关系如图所示。
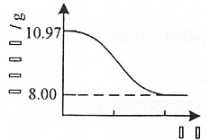
已知: 8.00g固体为黑色纯净物。
有关物质的摩尔质量如表:
物质 | CuCO3·Cu(OH)2 | CuCO3·2Cu(OH)2 | CuO |
摩尔质量/g·mol-1 | 222 | 320 | 80 |
请计算产品的纯度(写出计算过程,结果保留3位有效数字)。______
【题目】某化学小组欲探究NO![]() 的氧化性及其还原产物。
的氧化性及其还原产物。
(1)提出问题
甲同学认为只有溶液中同时存在H+时,NO![]() 才有氧化性;
才有氧化性;
乙同学不赞成甲同学观点,他认为NO![]() 自身就具有氧化性,依据是__________
自身就具有氧化性,依据是__________
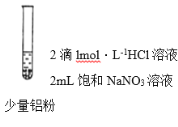
(2)实验探究:小组同学为解决上述争论,设计并进行了以下实验
实验I | 实验II | 实验III | |
操作 |
|
|
|
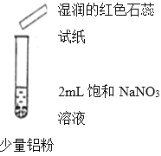
现象 | 微热,产生无色气泡,至液面上方变为浅红棕色。用拇指堵住试管口片刻,靠近酒精灯火焰,没有爆鸣声。 | 微热,产生无色气泡,湿润的红色石蕊试纸变蓝。用拇指堵住试管口片刻,靠近酒精灯火焰,没有爆鸣声。 | 微热,产生无色气泡,湿润的红色石蕊试纸变蓝。用拇指堵住试管口片刻,靠近酒精灯火焰,没有爆鸣声。 |
①实验I中反应的离子方程式为_________。
②实验II滴加两滴蒸馏水的目的是__________,产生的无色气泡为___________
③实验III反应后静置,取上层清液,滴加稀盐酸,先产生白色浑浊,后又消失。则实验III中反应的离子方程式为__________。
(3)实验结论:由实验I、II、III可得出的结论是________。