��Ŀ����
����Ŀ�����������FexNy���ڴż�¼�����������Ź㷺��Ӧ��ǰ����ijFexNy���Ʊ���������������ͪ���Ҵ����롣
��1����ͪ(CH3COCH3)������2��̼ԭ�ӹ�����ӻ�������__��1mol��ͪ�����к�����������ĿΪ___mol��
��2��C��H��O����Ԫ�صĵ縺����С�����˳��Ϊ__��������дԪ�����ƣ���Ҫ���κ����ӷ��ţ�
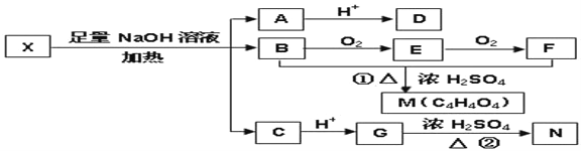
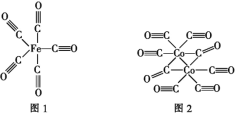
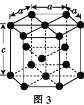
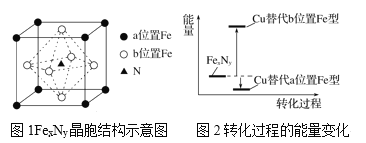
��3��ijFexNy�ľ�����ͼ1��ʾ��Cu������ȫ����þ�����aλ��Fe����bλ��Fe���γ�Cu����Ͳ���Fe(x��n)CunNy��FexNyת��Ϊ����Cu����Ͳ���������仯��ͼ2��ʾ�����и��ȶ���Cu����Ͳ���Ļ�ѧʽΪ__��
���𰸡�sp2 9 ��̼�� Fe3CuN
��������
��1��![]() �е�����Ϊ������˫���к�1������������C�γ�4��������C=O��C�γ�3��������
�е�����Ϊ������˫���к�1������������C�γ�4��������C=O��C�γ�3��������
��2���ǽ�����Խǿ���縺��Խ��
��3����ͼ2��֪��Cu���aλ�õ�Feʱ�����ϵͣ����ȶ�����Cuλ�ڶ��㣬N��Cu��=8��![]() =1��Feλ�����ģ�N��Fe��=6��
=1��Feλ�����ģ�N��Fe��=6��![]() =3��Nλ�����ġ�
=3��Nλ�����ġ�
��1��![]() �е�����Ϊ������˫���к�1������������C�γ�4��������C=O��C�γ�3��������2��̼Ϊ�ʻ���C��Ϊsp2�ӻ�������CΪsp3�ӻ���1mol��ͪ����9mol�������ʴ�Ϊ��sp2��9��
�е�����Ϊ������˫���к�1������������C�γ�4��������C=O��C�γ�3��������2��̼Ϊ�ʻ���C��Ϊsp2�ӻ�������CΪsp3�ӻ���1mol��ͪ����9mol�������ʴ�Ϊ��sp2��9��
��2���ǽ�����Խǿ���縺��Խ����C.H��O����Ԫ�صĵ縺����С�����˳��Ϊ��̼�����ʴ�Ϊ����̼����
��3����ͼ2��֪��Cu���aλ�õ�Feʱ�����ϵͣ����ȶ�����Cuλ�ڶ��㣬N��Cu��=8��![]() =1��Feλ�����ģ�N��Fe��=6��
=1��Feλ�����ģ�N��Fe��=6��![]() =3��Nλ����������ֻ��1��N���仯ѧʽΪFe3CuN���ʴ�Ϊ��Fe3CuN��
=3��Nλ����������ֻ��1��N���仯ѧʽΪFe3CuN���ʴ�Ϊ��Fe3CuN��

 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�����Ŀ�������ƣ�NaBiO3���Ƿ�����ѧ�е���Ҫ�Լ�����ˮ�л����ֽ⣬����ˮ������Ѹ�ٷֽ⡣ij��ȤС�����ʵ����ȡ�����Ʋ�̽����Ӧ�á��ش��������⣺
��.��ȡ������
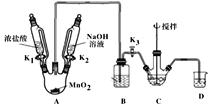
��ȡװ����ͼ�����Ⱥͼг���������ȥ�������������������£�
���� | NaBiO3 | Bi(OH)3 |
���� | ��������ˮ��dz��ɫ | ������ˮ����ɫ |
��1��Bװ�����ڳ�ȥHCl��ʢ�ŵ��Լ���___��
��2��C��ʢ��Bi(OH)3��NaOH������Cl2��Ӧ����NaBiO3����Ӧ�����ӷ���ʽΪ___��
��3�����۲쵽___��������ʱ�����Գ����ж�C�з�Ӧ�Ѿ���ɣ�
��4�����װ��ǰ�����ȳ�ȥ��ƿ�в���Cl2������Ⱦ��������ȥCl2�IJ�����___��
��5����Ӧ������Ϊ��װ��C�л�þ����ܶ�IJ�Ʒ����Ҫ�IJ�����___��
��.�����Ƶ�Ӧ����������Mn2+
��6��������Һ�м��������ƾ��壬�������ữ����Һ��Ϊ�Ϻ�ɫ��֤������Һ�д���Mn2+��
�ٲ����Ϻ�ɫ��������ӷ���ʽΪ___��
��ijͬѧ�ڽ�Ũ��MnSO4��Һ�м��������ƾ��壬�������ữ�����û���Ϻ�ɫ���֣����۲쵽��ɫ���壨MnO2�����ɡ���������������ӷ�Ӧ����ʽΪ___��
��.��Ʒ���ȵIJⶨ
��7��ȡ����NaBiO3��Ʒwg����������ϡ�����MnSO4ϡ��Һʹ����ȫ��Ӧ������cmo1��L-1��H2C2O4����Һ�ζ����ɵ�MnO4-����֪��H2C2O4+MnO4-����CO2+Mn2++H2O��δ��ƽ��������Һ�Ϻ�ɫǡ����ȥʱ������vmL����Һ��
�ò�Ʒ�Ĵ���Ϊ___���ú�w��c��v�Ĵ���ʽ��ʾ����