题目内容
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.向1 L 1 mol·L-1 NaClO溶液中通入足量CO2,溶液中HClO的分子数为NA
B.标准状况下,体积均为2.24 L的CH4与H2O含有的电子总数均为NA
C.2 mol NO与1 mol O2在密闭容器中充分反应,产物的分子数为2NA
D.由13 g乙酸与2 g CO(NH2)2(尿素)形成的混合物中含有的氢原子总数为NA
【答案】D
【解析】
A. 向1 L 1 mol·L-1 NaClO溶液中通入足量CO2,次氯酸是弱酸,部分电离,溶液中HClO的分子数小于NA,故A错误;
B. 标准状况下, H2O是液体,2.24 L H2O的物质的量不是0.1mol,故B错误;
C. NO和O2反应生成NO2,体系中存在![]() 平衡, 2 mol NO与1 mol O2在密闭容器中充分反应,产物的分子数小于2NA,故C错误;
平衡, 2 mol NO与1 mol O2在密闭容器中充分反应,产物的分子数小于2NA,故C错误;
D. 乙酸、CO(NH2)2中氢元素质量分数都是![]() ,由13 g乙酸与2 g CO(NH2)2(尿素)形成的混合物中含有的氢原子物质的量是
,由13 g乙酸与2 g CO(NH2)2(尿素)形成的混合物中含有的氢原子物质的量是![]() ,氢原子数是NA,故D正确。
,氢原子数是NA,故D正确。
选D。

 ABC考王全优卷系列答案
ABC考王全优卷系列答案【题目】(1)t1 ℃时,密闭容器中,通入一定量的CO和H2O,发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。容器中各物质浓度(单位: mol·L-1)变化如下表所示:
CO2(g)+H2(g) ΔH<0。容器中各物质浓度(单位: mol·L-1)变化如下表所示:
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
①一定处于平衡状态的时间段为____________。
②5~6 min时间段内,平衡移动方向为_______________ (填“向左移动”或“向右移动”),根据表中数据判断,平衡移动的原因是________(填字母编号)。
a.增加了H2O(g)的量 b.增加氢气浓度 c.使用催化剂 d.降低温度
③t2 ℃时(t2>t1),在相同条件下发生上述反应,达平衡时,CO浓度________c1(填“>”“<”或“=”)。
(2)已知反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
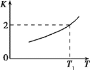
①用CO还原FeO制备Fe的反应是___________ (填“吸热”或“放热”)反应。
②温度为T2时,实验测得该反应体系中CO浓度为CO2的2.5倍,则T2______T1(填“>”“<”或“=”)。
(3)工业上常用CO、CO2和H2合成甲醇燃料,其原理为:
①CO(g)+2H2(g)![]() CH3OH(g) ΔH<0;②CO2(g)+H2(g)
CH3OH(g) ΔH<0;②CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH>0
CO(g)+H2O(g) ΔH>0
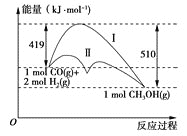
当混合气体的组成固定时,CO平衡转化率(α)与温度和压强的关系如图所示。
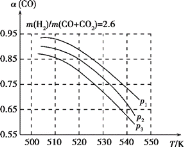
图中的压强由大到小的顺序为____________,判断理由是_________________________;
试解释CO平衡转化率随温度升高而减小的原因是_______________________。
【题目】铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
制取装置如图(加热和夹持仪器已略去),部分物质性质如下:

物质 | NaBiO3 | Bi(OH)3 |
性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(1)B装置用于除去HCl,盛放的试剂是___;
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为___;
(3)当观察到___(填现象)时,可以初步判断C中反应已经完成;
(4)拆除装置前必须先除去烧瓶中残留Cl2以免污染空气。除去Cl2的操作是___;
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有___;
Ⅱ.铋酸钠的应用——检验Mn2+
(6)往待测液中加入铋酸钠晶体,加硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+。
①产生紫红色现象的离子方程式为___;
②某同学在较浓的MnSO4溶液中加入铋酸钠晶体,加硫酸酸化,结果没有紫红色出现,但观察到黑色固体(MnO2)生成。产生此现象的离子反应方程式为___。
Ⅲ.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用cmo1·L-1的H2C2O4标准溶液滴定生成的MnO4-(已知:H2C2O4+MnO4-——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。
该产品的纯度为___(用含w、c、v的代数式表示)。