��Ŀ����
����Ŀ����ҵ���������Դ�����������ã����Ը����ȵط���ԭ���ϵļ�ֵ��ij��ʦ��ָ��ѧ�����о���ѧϰʱ�������÷���м��ʵ�����Ʊ�FeSO4��Һ����������ʵ�����(NH4)2SO4��Ӧ���Ʊ���Ѫ����������茶���[(NH4)2Fe(SO4)2��6H2O����Է�������Ϊ392]����������茶����һ���������ȶ����ڿ����в��ױ�������������ˮ���������Ҵ���
(1)����м�ľ�����������мͶ��10%��̼������Һ�в�����5~10min��ͨ����������ȥ������Һ����������ˮϴ������м�����á�
(2)���������ķ���м����2gFe�ۡ�10mL3mol��L-1��H2SO4��Һ������ƿ�з�Ӧ������ͼ��ʾװ���Ʊ�FeSO4��Һ�������¶�70~80�棬�ʵ�����ˮ�Բ��䱻��������ˮ�֣���������Һ��pH������Ӧ���������ݲ�����ֹͣ���ȣ����ˣ�������������������
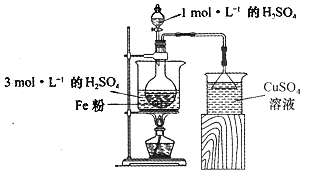
�ٷ�Ӧ�����л��������H2S��PH3�����壬��ʹ�÷��װ�á�д����CuSO4��Һ����H2S����Ļ�ѧ��Ӧ����ʽ��____________________________
�ڷ�Ӧ������ʹ�ù������۵�Ŀ����____________________________
(3)�Ʊ�(NH4)2Fe(SO4)2��6H2O����FeSO4��Һ�м���һ��������(NH4)2SO4���壬70~80���������ܽ���ȵ���50mL�Ҵ��У��������塣
ʵ���У���Թ��˳���Ʒ��ĸҺ(pH<1)���д����������£��ֱ�ȡĸҺ�������м���ָ�����ʣ���Ӧ�����Һ����Ҫ���ڵ�һ��������ȷ����_____ (�����)��
A.ͨ�����Cl2��Fe2+��H+��NH4+��Cl����SO42��
B.�������KSCN��Һ��K+��NH4+��Fe3+��SO42����SCN��
C.�������NaOH��Һ��Na+��Fe2+��NH4+��SO42����OH��
D.�������NaClO��NaOH�Ļ����Һ��Na+��SO42����Cl����ClO����OH��
(4)��Ʒ���Ȳⶨ����ȡag��Ʒ����ˮ�����Ƴ�500mL��Һ��ȡ25.00mL����Һ����Ũ��Ϊcmol��L-1������KMnO4��Һ�ζ����ظ���������2��ʵ�������£�

�ò�Ʒ�Ĵ���Ϊ____________________________(�ú�a��c�Ĵ���ʽ��ʾ)��
��ͬѧ������ⶨ��Ʒ��SO42���ĺ���Ҳ�ɲⶨ��Ʒ�Ĵ��ȣ��벹������ʵ�鷽������ȡԼ0.4g��Ʒ������70mLˮ��__________________________________________________���������������������������أ���¼����(ʵ���б���ʹ�õ��Լ��У�2mol��L-1��HCl��Һ��BaCl2��Һ��AgNO3��Һ)��
���𰸡�CuSO4+H2S=CuS��+H2SO4 ����Fe2+������ΪFe3+ D 980c/a��100% ����2mol/LHCl��Һ�ữ���μ�BaCl2��Һ��������ȫ�����ˣ�ϴ�ӳ�����ֱ����Һ�μ�AgNO3��Һ�����ֻ���
��������
��2����ʵ������CuSO4��Һ����H2S���壬�����������ͭ��
�����۾��л�ԭ�ԣ���Ӧ������ʹ�ù������۵�Ŀ���DZ���Fe2+������ΪFe3+��
��3���������ӹ�����жϷ������н�����
��4����һ����ڶ��Ρ����������ϴ��Բ��ƣ����ĸ��������Һ�����Ϊ��25.02+24.98��/2mL=25mL���������ӷ�Ӧ����ʽ���м������ⶨ��Ʒ��SO42���ĺ���Ҳ�ɲⶨ��Ʒ�Ĵ��ȣ�����ʵ�鷽��Ϊ����ȡԼ0.4g��Ʒ������70mLˮ������2mol/LHCl��Һ�ữ���μ�BaCl2��Һ��������ȫ�����ˣ�ϴ�ӳ�����ֱ����Һ�μ�AgNO3��Һ�����ֻ��ǣ��������������������������أ���¼������
��2����ʵ������CuSO4��Һ����H2S���壬�����������ͭ����ѧ��Ӧ����ʽΪ��CuSO4+H2S=CuS��+H2SO4���ʴ�ΪCuSO4+H2S=CuS��+H2SO4��
�����۾��л�ԭ�ԣ���Ӧ������ʹ�ù������۵�Ŀ���DZ���Fe2+������ΪFe3+���ʴ�Ϊ����Fe2+������ΪFe3+��
��3������֪��Ϣ��֪��ĸҺ����Ҫ���ڵ�������Fe2+��H+��NH4+��SO42����
A.ͨ�����Cl2����Һ�е�Fe2+���ܴ������棬����Ҫ���ڵ�����Ӧ����ClO-����A����
B.�������KSCN��Һ����Һ�е�Fe3+��SCN�����ܴ������棬��B����
C.�������NaOH��Һ����Һ�е�Fe2+��NH4+�����ܴ������ڣ���C����
D.�������NaClO��NaOH�Ļ����Һ��H+��OH�������кͷ�Ӧ����ˮ��NH4+��NH3����ʽ�ݳ���Fe2+��ת��ΪFe3+����2Fe2++ClO-+H2O=2Fe3++Cl-+2OH-��������Fe(OH)3����ʽ��ȥ����Ӧ�����Һ����Ҫ���ڵ�����Ϊ��Na+��SO42����Cl����ClO����OH������D��ȷ��
�ʴ�ΪD��
��4����Ϊ��һ����ڶ��Ρ����������ϴ��Բ��ƣ����ĸ��������Һ�����Ϊ��25.02+24.98��/2mL=25mL���������ӷ�Ӧ����ʽ���ó���n[��NH4��2SO4FeSO46H2O]=5n��KMnO4��=25��10-3��c��5mol����500mL��Һ�к���n[��NH4��2SO4FeSO46H2O]=25��10-3��c��5��500/25mol=2.5cmol�����Ըò�Ʒ����������=2.5c��392/a��100%=980c/a��100%��
�ⶨ��Ʒ��SO42���ĺ���Ҳ�ɲⶨ��Ʒ�Ĵ��ȣ�����ʵ�鷽��Ϊ����ȡԼ0.4g��Ʒ������70mLˮ������2mol/LHCl��Һ�ữ���μ�BaCl2��Һ��������ȫ�����ˣ�ϴ�ӳ�����ֱ����Һ�μ�AgNO3��Һ�����ֻ��ǣ��������������������������أ���¼�������ʴ�Ϊ980c/a��100%������2mol/LHCl��Һ�ữ���μ�BaCl2��Һ��������ȫ�����ˣ�ϴ�ӳ�����ֱ����Һ�μ�AgNO3��Һ�����ֻ�����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�