��Ŀ����
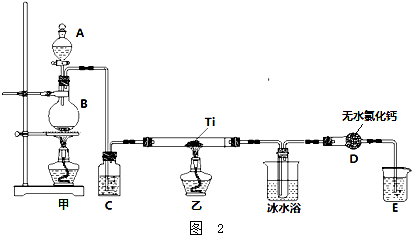
2��ij��ѧ����С��������ͼװ����ȡ�屽�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A�У�A�¶˻����رգ���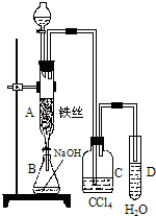
д��A�з�Ӧ�Ļ�ѧ����ʽ2Fe+3Br2=2FeBr3��C6H6+Br2$\stackrel{FeBr_{3}}{��}$C6H5Br+HBr��A��Һ���У�������ɫ����������÷�Ӧ�Ƿ��ȷ�Ӧ������ȡ������ȡ�������ɫ����ijɷ���Br2��ʵ�����ʱ����A�¶˵Ļ������÷�ӦҺ����B�г����Ŀ���dz�ȥ�����屽�е���д���йط�Ӧ�Ļ�ѧ����ʽBr2+2NaOH=NaBr+NaBrO+H2O������3Br2+6NaOH=5NaBr+NaBrO3+3H2O��C��ʢ��CCl4�������dz�ȥ�廯�������е�����������Ƽ�ʵ��֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ����������֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ�������Թ�D�е���AgNO3��Һ������������ɫ����������֤������һ����֤�ķ��������Թ�D�м���ʯ����Һ����������Һ���ɫ��
���� ���ʹ��������Ȼ������������£�������һ����ԭ�ӷ���ȡ����Ӧ�����屽���廯�⣻��������һ�ֺ���ɫ�����壬A��Һ���У�������ɫ����������÷�Ӧ�Ƿ��ȷ�Ӧ����ɫ����ijɷ����ӷ����嵥�ʣ�����Һ����ӷ������������屽���������������������Ʒ�Ӧ���屽���ܣ�CCl4 ���ܽ��岻���ܽ��廯�⣻�������Һ�巢������ȡ����Ӧ������HBr���ɣ��廯��������ˮ�����H+��Br-�����������������ӻᷢ����Ӧ����AgBr����������������Ǽӳɷ�Ӧ������HBr���ɣ�
��� �⣺���ʹ��������廯�����������£�������һ����ԭ�ӷ���ȡ����Ӧ�����屽���廯�⣬��ӦΪ��2Fe+3Br2=2FeBr3��C6H6+Br2$\stackrel{FeBr_{3}}{��}$C6H5Br+HBr��
����Һ����ӷ�����������һ�ֺ���ɫ�����壬A��Һ���У�˵���÷�Ӧ�Ƿ��ȷ�Ӧ��������ɫ�������������������һ��˵���÷�Ӧ�Ƿ��ȷ�Ӧ��
A�е�����������Ʒ�Ӧ�����Խ��屽�е����ȥ����Br2+2NaOH=NaBr+NaBrO+H2O������3Br2+6NaOH=5NaBr+NaBrO3+3H2O��
CCl4���ܽ��岻���ܽ��廯�⣬���Ȼ�̼�ܳ�ȥ�廯�������е���������
��֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ�������ǣ��������ȡ����Ӧ�������廯�⣬�廯��������ˮ�����H+��Br-��ֻҪ���麬�������ӻ������Ӽ��ɣ������ӵļ��飺ȡ��Һ�μ���������Һ��������ɵ���ɫ������֤���������ӣ������ӵļ��飺�����ʹ��ɫʯ����Һ��죬��֤�����������ӣ�
�ʴ�Ϊ��2Fe+3Br2=2FeBr3��C6H6+Br2$\stackrel{FeBr_{3}}{��}$C6H5Br+HBr�����ȣ�Br2����ȥ�����屽�е��壻Br2+2NaOH=NaBr+NaBrO+H2O������3Br2+6NaOH=5NaBr+NaBrO3+3H2O����ȥ�廯�������е�����������֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ�������Թ�D�е���AgNO3��Һ������������ɫ����������֤������һ����֤�ķ��������Թ�D�м���ʯ����Һ����������Һ���ɫ��
���� ���⿼�鱽��ȡ����Ӧ����ʽ��ʵ�������Լ�����HBr�ļ��飬��Ŀ�Ѷ��еȣ�ע�����ձ���ȡ����Ӧԭ������ȷ��Ӧ�IJ��PHBr�Ļ�ѧ���ʽ��н��⣮

 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�| A�� | 1 mol•L-1 HCl��Һ��c��Cl-����c��H+����c��OH-�� | |
| B�� | 1 mol•L-1 Na2CO3��Һ��c��Na+��+c��H+��=2c��CO32-��+c��HCO3-��+c��OH-�� | |
| C�� | 1 mol•L-1 NaHCO3��Һ��c��H+��+2c��H2CO3��=c��OH-��+c��CO32-�� | |
| D�� | 0.1 mol•L-1NaOH��Һ������pH=1�Ĵ����Ϻ����Һ�У�c ��CH3COO-��=c ��Na+����c ��H+��=c ��OH-�� |
| A�� | NH3�к��е�3��N-H���ǵ�ͬ�� | B�� | NH3��N-H��֮��ļн�Ϊ107��18�� | ||
| C�� | NH3���ӿռ乹��Ϊ������ | D�� | NH3���۵��ˮ���۵�� |
��Ӧ��Ͳ���IJ������������ʾ��
| ���� | ������ | ��״ | �ܶ�g/cm3 | �۵�� | �е�� | �ܽ�ȣ���/100mL�ܼ� | ||
| ˮ | �� | �� | ||||||
| ����ȩ | 106 | ��ɫҺ�� | 1.06 | -26 | 178 | 0.3 | ���� | ���� |
| ������ | 102 | ��ɫҺ�� | 1.082 | -73 | 138 | 12 | �� | ���� |
| ����� | 148 | ��ɫ���� | 1.248 | 133 | 300 | 0.04 | 24 | �� |

��Ҫʵ�鲽�裺
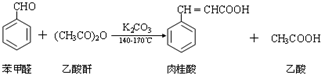
��ϳɣ���ͼ����������������5mL����ȩ��14mL��������7.0g��ˮ̼��أ��ټ��뼸������X�������¶���140��170�棬���˻�������45min��
��������ᴿ��
�ٽ������ϳɵIJ�Ʒ��ȴ��߽������40mLˮ����5���ӣ�����ˮ�������ӻ�����г�ȥδ��Ӧ�ı���ȩ���õ��ֲ�Ʒ
�ڽ������ֲ�Ʒ��ȴ�����40mL 10%����������ˮ��Һ���ټ�90mLˮ�����Ȼ���̿��ɫ�����ȹ��ˡ���ȴ��
�۽�1��1�������ڽ����¼��뵽���������Һ�У�����Һ�����ԣ�����ȴ�����ˡ�ϴ�ӡ�
����Ȳ����õ��ϴ����������4.5�ˣ�
��ش��������⣺
��1������X�������Ƿ�ֹ���У�X�������Ƿ�ʯ�����Ƭ
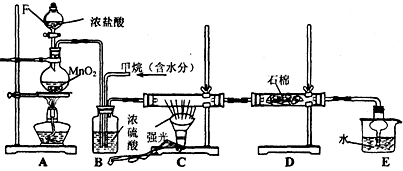
��2��ͼ��װ���������ܵ��������������������ԭ�������ʣ����ٲ���ӷ�
��3��ͼ��װ���в����ܵ�������ƽ��ѹǿ������D����������ƿ
��4���ϳ�������ʵ��������ˮ�����½��У�ʵ��ǰ����������ʵ����Ϊ�����¶���140��170������BD�м��ȣ��������ѡ����ѡ��
A��ˮ B�����ͣ��е�290�棩 C��ɰ�� D��ֲ���ͣ��е�230��325�棩
��5����ʵ���У������IJ���Ϊ60.8%��
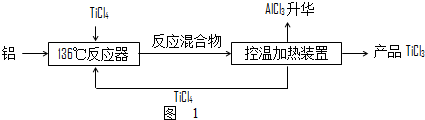
 $\stackrel{���ʵ�������}{��}$
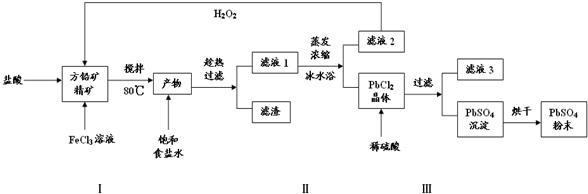
$\stackrel{���ʵ�������}{��}$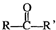 ��ע��R��R��Ϊ��������AΪ�л��ϳ��м��壬��һ�������·�����ȥ��Ӧ�����ܵõ����ֻ�Ϊͬ���칹��IJ�����е�һ��B��������ȡ�ϳ���֬��Ⱦ�ϵȶ��ֻ�����Ʒ��A�ܷ�����ͼ��ʾ�ı仯��
��ע��R��R��Ϊ��������AΪ�л��ϳ��м��壬��һ�������·�����ȥ��Ӧ�����ܵõ����ֻ�Ϊͬ���칹��IJ�����е�һ��B��������ȡ�ϳ���֬��Ⱦ�ϵȶ��ֻ�����Ʒ��A�ܷ�����ͼ��ʾ�ı仯��
 ��
�� ��
�� ��
��