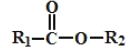题目内容
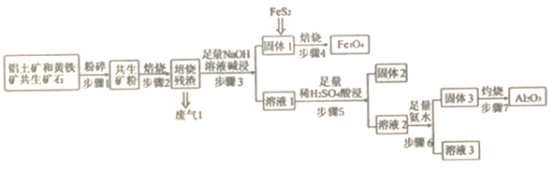
【题目】氯化亚铜为白色粉末状固体,难溶于水和乙醇,潮湿时易被氧化,可用作催化剂、杀菌剂、媒染剂等。工业以硫化铜精矿为原料,制备氯化亚铜的流程如图:

下列说法正确的是( )
A.步骤①焙烧产生的有毒气体可用碱液吸收
B.步骤②所用硫酸浓度越大浸出速率越快
C.步骤③离子方程式:![]()
D.步骤④用乙醇洗涤的目的是使![]() 尽快干燥,防止被空气氧化
尽快干燥,防止被空气氧化
【答案】AD
【解析】
A.步骤①焙烧硫化铜,产生的有毒气体SO2可用碱液吸收,A正确;
B.步骤②所用硫酸浓度过大,会对后续加入Na2SO3还原Cu2+产生干扰,B错误;
C.在硫酸铜中加入Na2SO3和NaCl,倾出清液,抽滤即得CuCl沉淀发生氧化还原反应,反应的离子方程式为:2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H﹢,C错误;
D.由题中信息可知,氯化亚铜难溶于水和乙醇,潮湿时易被氧化,因此,步骤④用乙醇洗涤的目的有利加快去除CuCl表面水分,防止其被空气中的氧气氧化,D正确。
答案选AD。

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目