题目内容
【题目】CO2 与 H2 合成(CH3)2O(二甲醚)是煤化工中的重要反应,有关信息如下:2CO2(g)+6H2(g) ![]() (CH3)2O(g)+3H2O(g) ΔH<0 恒容下,该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是( ) (K 表示该反应的平衡常数)
(CH3)2O(g)+3H2O(g) ΔH<0 恒容下,该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是( ) (K 表示该反应的平衡常数)
A.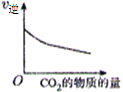 B.
B.
C.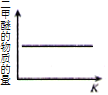 D.
D.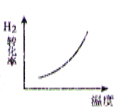
【答案】B
【解析】
分析反应可知,该反应正向放热、气体的物质的量减少,根据这些特点,结合勒夏特列原理,可对该反应的平衡进行判断。
A.恒容条件下增大二氧化碳的物质的量,即增大反应物二氧化碳的物质的量浓度,使正反应速率增大,平衡正向移动,而逆反应速率初始不变,随后逐渐增大,直至建立新的平衡,A选项错误。
B.该反应放热,随温度的升高,平衡逆向移动,气体的物质的量增加,恒容条件下压强增大;另:升温也能使气体压强增大,B选项正确。
C.平衡常数只受温度影响。该反应放热,平衡常数增大过程即为降温过程。随平衡常数的增大,温度降低,平衡正向移动,二甲醚的物质的量增加,C选项错误。
D.反应放热随温度的升高平衡向逆向移动,氢气的转化率下降,D选项错误。
答案选B。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目