题目内容
如图所示,a、b、c均为石墨电极,d为碳钢电极, 通电进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是
| A.甲、乙两烧杯中溶液的pH均保持不变 |
| B.甲烧杯中a的电极反应式为:4OH――4e- = O2↑+2H2O |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 |
| D.当b极增重3.2g时,d极产生的气体为2.24L(标准状况下) |
B
解析试题分析:A、a电极上由水电离出的氢氧根离子放电生成氧气,导致a电极附近氢离子浓度增大,b电极上铜离子放电生成铜,所以甲中pH减小;c电极上氯离子放电生成氯气,d电极上由水电离出的氢离子放电生成氢气,导致d电极附近氢氧根离子浓度增大,溶液的pH增大,故A错误;B、甲中,a极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=O2↑+2H2O,故B正确;C、当电解一段时间后,甲中溶质含有硫酸,可能含有硫酸铜,乙中含有氢氧化钠,可能含有氯化钠,二者混合时,可能产生氢氧化铜沉淀,故C错误;D、当b极增重3.2g时,铜离子得到电子的物质的量=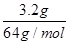 ×2=0.1mol,串联电路中转移电子相等,d极产生的气体体积=
×2=0.1mol,串联电路中转移电子相等,d极产生的气体体积=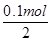 ×22.4L/mol=1.12L,故D错误,故答案选B。
×22.4L/mol=1.12L,故D错误,故答案选B。
考点:考查原电池和电解池的工作原理以及有关计算

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案汽车等机动车辆的启动电源常用铅蓄电池,放电时的电池反应如下:
PbO2+Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是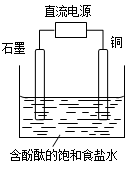
| A.铜电极附近观察到黄绿色气体 |
| B.石墨电极附近溶液呈红色 |
| C.溶液中的Na+向石墨电极移动 |
| D.铜电极上发生还原反应 |
某兴趣小组设计如图所示的微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为:2H+ + 2Cl- Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,石墨电极附近溶液变红 |
| C.断开K1,闭合K2时,铜电极上的电极反应为: Cl2+2e-=2Cl- |
| D.断开K1,闭合K2时,石墨电极作正极 |
用酸性氢氧燃料电池为电源进行电解的实验装置图如图所示,下列说法中正确的是( )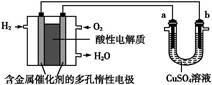
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
两种金属A与B组成原电池时,A是正极。下列有关推断正确的是( )
| A.A的金属性强于B |
| B.A电极上发生的电极反应是还原反应 |
| C.电子不断由A电极经外电路流向B电极 |
| D.A在金属活动性顺序表中一定排在氢前面 |
下列关于电化学知识说法正确的是( )
| A.电解AlCl3、FeCl3、CuCl2的混合溶液,在阴极上依次析出Cu、Fe、Al |
| B.电解CuSO4溶液一段时间后,加入适量Cu(OH)2可以使溶液恢复至原状态 |
| C.铅蓄电池在充电时,连接电源正极发生的电极反应为PbSO4+2e-=Pb+SO42- |
| D.将钢闸门与直流电流的负极相连,可防止钢闸门腐蚀 |
根据图所示装置,下列说法不正确的是( )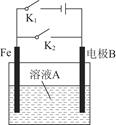
| 选项 | 开关状态 | 溶液A | 电极B | 说明 |
| A | 打开K1,闭合K2 | NaCl | 石墨 | 正极反应:O2+2H2O+4e-=4OH- |
| B | 打开K1,闭合K2 | NaCl | Zn | 铁制品保护:牺牲阳极的阴极保护法 |
| C | 打开K2,闭合K1 | CuSO4 | Cu | 铁表面镀铜 |
| D | 打开K2,闭合K1 | CuSO4 | 粗铜 | 电解法精炼铜 |
电化学在日常生活中用途广泛,图①是镁次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O72-的工业废水的处理。下列说法正确的是( )
| A.图②中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图①中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ |
| D.若图①中3.6 g镁溶解产生的电量用于图②废水处理,理论可产生10.7 g氢氧化铁沉淀 |