题目内容
(1)KClO3+6HCl=KCl+3Cl2↑+3H2O中氧化剂是 ,还原剂是 ,请用双线桥表示电子转移数目 .当有1mol Cl2生成时,氧化剂与还原剂的物质的量之比为 .
(2)3NO2+H2O=2HNO3+NO中当电子转移4mol时,参加还原反应的NO2有 mol,氧化产物与还原产物物质的量之比为 .
(2)3NO2+H2O=2HNO3+NO中当电子转移4mol时,参加还原反应的NO2有
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子;
(2)3NO2+H2O=2HNO3+NO中,只有N元素的化合价变化,由生成NO可知,生成1molNO时转移2mol电子,以此来解答.
(2)3NO2+H2O=2HNO3+NO中,只有N元素的化合价变化,由生成NO可知,生成1molNO时转移2mol电子,以此来解答.
解答:
解:(1)反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,KClO3为氧化剂,HCl为还原剂,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为 ,当有1mol Cl2生成时,氧化剂与还原剂的物质的量之比为
,当有1mol Cl2生成时,氧化剂与还原剂的物质的量之比为
mol:
mol=1:5,
故答案为:KClO3;HCl; ;1:5;
;1:5;
(2)3NO2+H2O=2HNO3+NO中,只有N元素的化合价变化,由生成NO可知,生成1molNO时转移2mol电子且有3molNO2反应,当电子转移4mol时,参加还原反应的NO2有6mol,HNO3为氧化产物,NO为还原产物,由反应可知,氧化产物与还原产物物质的量之比为2:1,故答案为:6;2:1.
 ,当有1mol Cl2生成时,氧化剂与还原剂的物质的量之比为
,当有1mol Cl2生成时,氧化剂与还原剂的物质的量之比为| 1 |
| 3 |
| 5 |
| 3 |
故答案为:KClO3;HCl;
 ;1:5;
;1:5;(2)3NO2+H2O=2HNO3+NO中,只有N元素的化合价变化,由生成NO可知,生成1molNO时转移2mol电子且有3molNO2反应,当电子转移4mol时,参加还原反应的NO2有6mol,HNO3为氧化产物,NO为还原产物,由反应可知,氧化产物与还原产物物质的量之比为2:1,故答案为:6;2:1.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
相关题目
芳香族化合物A的分子式为C7H8O,它与Na反应有气体产生.满足条件的同分异构体的数目是( )
| A、4 | B、3 | C、2 | D、1 |
下列变化不符合科学原理的是( )
| A、稻草变酒精 | B、废塑料变汽油 |
| C、空气变肥料 | D、水变油 |
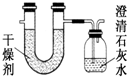 已知某种燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收).
已知某种燃料含有碳、氢、氧三种元素.为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收).
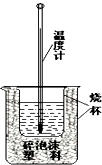 实验室利用如图装置进行中和热的测定,请回答下列问题:
实验室利用如图装置进行中和热的测定,请回答下列问题: