题目内容
11.金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用.请完成下列空白:(1)铝元素在周期表中的位置为第三周期第ⅢA族.
(2)在19世纪时,铝是一种珍贵的金属.人们最初得到的铝粒如同珍宝,它的价格同黄金相当.1827年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝.用钾与无水氯化铝反应制铝而不用氯化铝溶液的理由是钾先与水反应生成KOH,KOH再与氯化铝反应生成氢氧化铝,无法得到单质铝.现代工业炼铝的原料是通过碱溶法由铝土矿提取而得,在提取过程中通入的气体为CO2.
(3)火箭和导弹表面的薄层是耐高温物质.将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)$\frac{\underline{\;高温\;}}{\;}$2Al2O3(s)+3TiC(s)△H=-1176kJ.mol-1,则反应过程中,每转移1mol电子放出的热量为98 kJ.
(4)硅与铝同周期,地壳里硅铝的含量:硅>铝(填>,<或=).硅酸盐是玻璃 (Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O.CaO.6SiO2.盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式SiO2+2NaOH=Na2SiO3+H2O.长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同.由钠长石化学式NaAlSi3O8可推知钙长石的化学式为CaAl2Si2O8.
(5)用铝和金属氧化物反应制备金属单质是工业上较常用的方法.如:2Al+4BaO$\stackrel{高温}{?}$3Ba↑+BaO.Al2O3,利用化学平衡移动原理解释上述方法可制取金属Ba的原因是利用Ba的沸点比Al的低,Ba以气体逸出,使平衡右移.
分析 (1)Al的原子结构为 ,由原子结构可知位置;
,由原子结构可知位置;
(2)在溶液中K与水反应;氧化铝与强碱反应生成偏铝酸盐,再通二氧化碳可得氢氧化铝沉淀;
(3)由反应可知,转移12mol电子放出1176kJ热量;
(4)地壳里含量前三位的为氧、硅、铝;二氧化硅与NaOH溶液反应具有粘合性的硅酸钠;由钠长石化学式NaAlSi3O8可推知钙长石的化学式,只有Na、Ca的化合价不同;
(5)高温下,Ba为气体,从反应体系逸出.
解答 解:(1)Al的原子结构为 ,由原子结构可知位于第三周期第ⅢA族,故答案为:第三周期第ⅢA族;
,由原子结构可知位于第三周期第ⅢA族,故答案为:第三周期第ⅢA族;
(2)在溶液中钾先与水反应生成KOH,KOH再与氯化铝反应生成氢氧化铝,无法得到单质;氧化铝与强碱反应生成偏铝酸盐,再通二氧化碳可得氢氧化铝沉淀;现代工业炼铝的原料是通过碱溶法由铝土矿提取而得,即氧化铝与强碱反应生成偏铝酸盐,再通二氧化碳可得氢氧化铝沉淀,所以在提取过程中通入的气体为CO2;
故答案为:钾先与水反应生成KOH,KOH再与氯化铝反应生成氢氧化铝,无法得到单质;CO2;
(3)由反应可知,转移12mol电子放出1176kJ热量,则每转移1mol电子放出的热量为$\frac{1176}{12}$=98kJ,
故答案为:98kJ;
(4)地壳里含量前三位的为氧、硅、铝,则含量为硅>铝;二氧化硅与NaOH溶液反应具有粘合性的硅酸钠,反应为SiO2+2NaOH=Na2SiO3+H2O;由钠长石化学式NaAlSi3O8可推知钙长石的化学式,只有Na、Ca的化合价不同,则钙长石的化学式为CaAl2Si2O8,
故答案为:>;SiO2+2NaOH=Na2SiO3+H2O;CaAl2Si2O8;
(5)高温下,Ba为气体,从反应体系逸出,减少生成物,即利用Ba的沸点比Al的低,Ba以气体逸出,使平衡右移,
故答案为:利用Ba的沸点比Al的低,Ba以气体逸出,使平衡右移.
点评 本题考查较综合,涉及物质的性质、位置与结构、化学平衡移动原理的应用等,综合性较强,侧重分析与应用能力的综合考查,题目难度中等.

 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案| A. | H2S与SO2、NO与O2、NH3与Cl2在常温下均不能大量共存 | |
| B. | SiO2化学性质相对稳定,在一定条件下也能与某些非金属单质、酸、碱、盐反应 | |
| C. | Fe(OH)3、FeCl2、FeCl3、NO、H2SiO3均可通过化合反应得到 | |
| D. | AlCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 |
| 成分 | SiO2 | MgO | Fe2O3 | Al2O3 | CuO |
| 质量分数(%) | ? | 4.0 | 32 | 10.2 | 16 |
| Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀的pH | 4.8 | 9.3 | 2.7 | 3.8 |
| 完全沉淀的pH | 6.4 | 10.8 | 3.7 | 4.7 |

请回答下列问题:
(1)沉淀Ⅰ的主要用途是制光导纤维(列一种即可),步骤Ⅳ中调节pH范围为大于3.7小于4.8.
(2)由滤液Ⅱ经几步反应可得到需要制备的一种金属的氧化物,滤液Ⅱ中需要通入气体的化学式CO2,反应的化学方程式为AlO2-+CO2+2H2O=Al(OH)3+HCO3-.
(3)写出由滤液Ⅰ得到滤液Ⅱ的离子方程式Al3++4OH-═AlO2-+2H2O
(4)滤液Ⅳ中含有的金属阳离子是Mg2+,Cu2+.
(5)工业上,冶炼铝、铁、铜、镁的方法依次是B(填代号).
A.电解法、热还原法、分解法、分解法 B.电解法、热还原法、热还原法、电解法
C.热还原法、分解法、电解法、电解法 D.热还原法、热还原法、热还原法、电解法
根据上述流程图,冶炼金属时选择的相应物质的化学式依次是Al2O3、Fe2O3、CuO、MgCl2.
(6)现有10t上述矿渣,理论上,可以冶炼2.24t铁.
| A. | 1.5mol/L | B. | 2mol/L | C. | 1mol/L | D. | 无法确定 |
| A. | 用湿润的pH试纸来测溶液的pH | |
| B. | 用四氯化碳萃取溴的苯溶液中的溴 | |
| C. | 实验室将硫酸铜溶液直接加热蒸干来制取CuSO4•5H2O | |
| D. | 用KSCN溶液检验硫酸亚铁溶液是否氧化变质 |
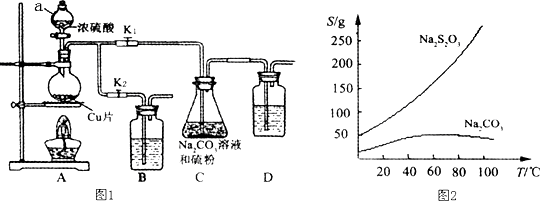
 二氧化氯(ClO2)气体是一种常用高效的自来水消毒剂.
二氧化氯(ClO2)气体是一种常用高效的自来水消毒剂.