题目内容
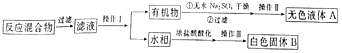
【题目】从海带中提取碘的工业生产过程如下:
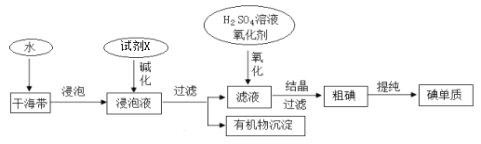
下列说法不正确的是 ( )
A.试剂X可以为NaOH溶液,其作用是使浸泡液中的可溶性有机物形成沉淀
B.氧化剂可以用H2O2或适量的Cl2
C.干海带浸泡液中的碘离子可用淀粉溶液检验
D.氧化后的滤液在实验室也可采用四氯化碳萃取、分液、蒸馏的方法得到粗碘
【答案】C
【解析】
A.海带浸泡后,加入氢氧化钠碱化后可过滤分离出有机物沉淀,便于分离,故正确;
B.氧化剂X可以用过氧化氢或适量的氯气,都可以氧化碘离子,故正确;
C.淀粉遇碘单质变蓝,但是碘离子不能使淀粉溶液变蓝,故错误;
D.因碘易溶于有机溶剂,氧化后的滤液在实验室可以采用四氯化碳萃取分液蒸馏的方法得到碘,整理后得到的粗碘在蒸馏烧瓶中,故正确。
故选C 。

练习册系列答案
相关题目