题目内容
【题目】将29.6g碳酸钠和碳酸氢钠的混合物加热到质量不再减少为止,冷却,称得固体质量为26.5g。问:
(1)原固体混合物中碳酸氢钠的质量是多少? ____________
(2)原固体混合物中碳酸钠的物质的量是多少?_____________
(3)把原固体混合物与足量盐酸完全反应生成的CO2在标准状况下的体积是多少?__________
【答案】8.4g 0.2 mol 6.72 L
【解析】
根据碳酸氢钠受热分解,产生水和二氧化碳,固体质量减少,据此计算碳酸氢钠的质量,进而求得碳酸钠的质量,再根据二者与酸反应时与二氧化碳的比例关系快速计算二氧化碳的物质的量以及标况下的体积。
(1)碳酸氢钠受热分解生成碳酸钠和水和二氧化碳,方程式为:
2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
168 62
m 29.6-26.5
有 ![]() ,解m=8.4g;
,解m=8.4g;
(2).碳酸钠的质量为29.6g-8.4g=21.2g,物质的量为 ![]() =0.2 mol;
=0.2 mol;
(3)根据碳酸钠和酸反应中碳酸钠和二氧化碳的比例为1:分析,0.2mol碳酸钠产生0.2mol二氧化碳,碳酸氢钠和酸反应时,碳酸氢钠和二氧化碳的比例为1;1,故8.4克碳酸氢钠产生0.1mol二氧化碳,即总共产生0.3mol二氧化碳,标况下的体积为0.3mol×22.4L/mol= 6.72 L。

 名师金手指领衔课时系列答案
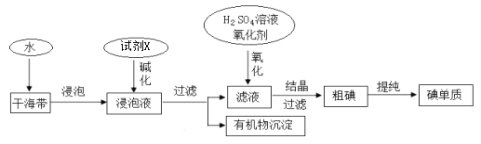
名师金手指领衔课时系列答案【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯, 易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ||
(1)用H2还原无水FeCl3制取FeCl2。有关装置如下:

①H2还原无水FeCl3制取FeCl2的化学方程式为_______。
②按气流由左到右的方向,上述仪器的连接顺序为____(填字母,装置可多次使用);C中盛放的试剂是_____。
③该制备装置的缺点为______。
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的名称是____。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是__,回收滤液中C6H5C1的操作方法是____。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/LNaOH溶液滴定,终点时消耗NaOH溶液为19.60 mL,则氯化铁的转化率为______。
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
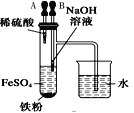
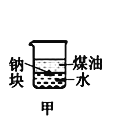
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是

①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D