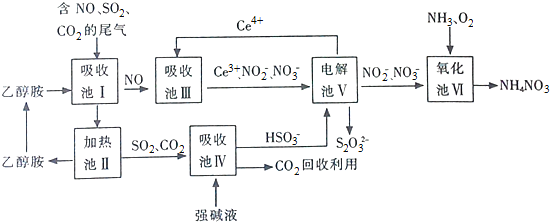
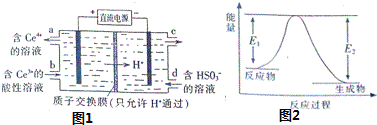
题目内容
【题目】(1)现有反应CO(g)+2H2(g)CH3OH(g)过程中能量变化如图所示,写出该反应的热化学方程式_____________________________;
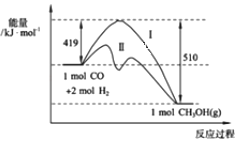
(2)已知该反应中相关的化学键键能数据如图所示,则C≡O中的键能为_____kJmol﹣1;图中曲线Ⅱ表示____________(填反应条件)的能量变化。
化学键 | H﹣H | C﹣O | H﹣O | C﹣H |
E/(kJmol﹣1) | 436 | 343 | 465 | 413 |
(3)图中数字“419”表示的是_________________________;
(4)下列反应中,属于放热反应的是_______ (填编号,下同),属于吸热反应的是_______;
①物质燃烧;②炸药爆炸;③酸碱中和反应;④二氧化碳通过炽热的碳;⑤食物因氧化而腐败;⑥Ba(OH)28H2O与NH4Cl反应;⑦铁粉与稀盐酸反应。
【答案】CO(g)+2H2(g)=CH3OH(g)△H=﹣91kJ/mol 1084 使用催化剂 反应的活化能或1molCO和2molH2断键所需要吸收的能量 ①②③⑤⑦ ④⑥
【解析】
(1)根据反应物与生成物的总能量来分析吸热还是放热,并书写热化学反应方程式;
(2)依据化学反应焓变=反应物键能总和-生成物键能总和计算C≡O中的键能,图中曲线Ⅱ表示降低了反应物的活化能,据此分析;
(3)根据图象分析判断数字“419”表示的含义;
(4)根据常见的放热反应和吸热反应分析判断。
(1)反应物的总能量与活化能的差值为419kJ,生成物的总能量与活化能的差值为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,故答案为:CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol;
(2)焓变=反应物键能总和-生成物键能总和,所以设C≡O中的键能为xkJ/mol,则-91=436×2+x-(413×3+343+465),解得:x=1084kJ/mol,图中曲线Ⅱ表示降低了反应物的活化能,所以曲线Ⅱ表示使用了催化剂的能量变化;故答案为:1084;使用了催化剂;
(3)图中数字“419”表示的是反应的活化能或1molCO和2molH2断键所需要吸收的能量,故答案为:反应的活化能或1molCO和2molH2断键所需要吸收的能量;
(4)①物质燃烧属于放热反应;②炸药爆炸属于放热反应;③酸碱中和反应属于放热反应;④二氧化碳通过炽热的碳虽然是化合反应,但属于吸热反应;⑤食物因氧化而腐败属于放热反应;⑥Ba(OH)28H2O与NH4Cl反应为吸热反应 ⑦铁粉与稀盐酸的反应属于放热反应;所以放热反应有:①②③⑤⑦;吸热反应有:④⑥,故答案为:①②③⑤⑦;④⑥。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】H2是一种重要的清洁能源。
(1)已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.1kJmol-1
CO2(g)+H2(g) ΔH3=-41.1kJmol-1
H2还原 CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
A.高温 B.低温 C.任何温度条件下
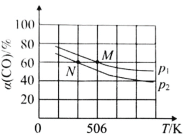
(2)恒温恒压下,在容积可变的密闭容器中加入 1molCO和2.2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
(3)若反应 CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是____(填字母);
A.容器内压强保持不变 B.2v正
C.混合气体的相对分子质量保持不变 D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=___(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=___kPamin-1。