题目内容
【题目】可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是:①一个N≡N键断裂的同时,有3个H—H键断裂;②一个N
2NH3已达到平衡状态的是:①一个N≡N键断裂的同时,有3个H—H键断裂;②一个N![]() N键断裂的同时,有6个N—H键断裂;③其他条件不变时,混合气体平均相对分子质量不再改变;④保持其他条件不变时,体系压强不再改变;⑤NH3%、N2%、H2%都不再改变;⑥恒温恒容时,密度保持不变;⑦正反应速率v(H2)=0.6 mol·(L·min)-1逆反应速率v(NH3)=0.4 mol·(L·min)-1。
N键断裂的同时,有6个N—H键断裂;③其他条件不变时,混合气体平均相对分子质量不再改变;④保持其他条件不变时,体系压强不再改变;⑤NH3%、N2%、H2%都不再改变;⑥恒温恒容时,密度保持不变;⑦正反应速率v(H2)=0.6 mol·(L·min)-1逆反应速率v(NH3)=0.4 mol·(L·min)-1。
A.全部B.①③④⑤C.②③④⑤⑦D.①③⑤⑥⑦
【答案】C
【解析】
①一个N≡N断裂的同时,有3个H-H键断裂,表示的都是正反应速率,无法判断正逆反应速率是否相等,故①错误;
②一个N≡N键断裂的同时,有6个N-H键断裂,正逆反应速率相等,达到了平衡状态,故②正确;
③反应过程中气体的总质量不会发生变化,但正反应是个气体分子数减小的反应,混合气体平均摩尔质量不再改变,说明气体总的物质的量不再改变即达到了平衡状态,故③正确;
④反应方程式两边气体的体积不相等,保持其它条件不变,当体系压强不再改变时,说明正逆反应速率相等,达到了平衡状态,故④正确;
⑤NH3、N2、H2的体积分数都不再改变,说明各组分的浓度不变,达到了平衡状态,故⑤正确;
⑥恒温恒容时,混合气体的密度保持不变,由于气体的质量不变,容器的容积不变,所以气体的密度始终不变,故密度不变时无法判断是否达到平衡状态,故⑥错误;
⑦正反应速率υ(H2)=0.6mol·L·min–1,逆反应速率υ(NH3)=0.4 mol·L·min–1,逆反应速率υ(H2)=0.6 mol·L·min–1,则氢气的正逆反应速率相等,达到了平衡状态,故⑦正确。
综上所述正确答案为C。

【题目】某化学研究性学习小组针对原电池形成条件,设计了实验方案,进行如下探究。
(1)请填写有关实验现象并得出相关结论。
编号 | 实验装置 | 实验现象 |
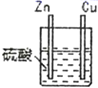
1 |
| 锌棒逐渐溶解,表面有气体生成;铜棒表面无现象 |
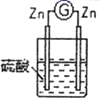
2 |
| 两锌棒逐渐溶解,表面均有气体生成;电流计指针不偏转 |
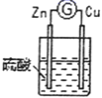
3 |
| 铜棒表面的现象是:有气体生成,电流计指针发生偏转 |
①通过实验2和3,可得出原电池的形成条件是______________;
②通过实验1和3,可得出原电池的形成条件是_______________;
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是_______;
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:______________;Cu棒:____________。