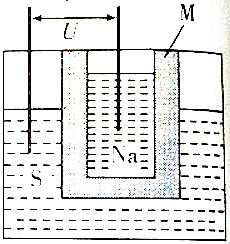
题目内容
5.在一定条件下,Ti和I2可以发生如下反应:Ti(s)+2I2(g)$→_{1300~1500℃}^{100~200℃}$ TiI4(g),下列说法正确的是( )| A. | 该反应△S>0 | |
| B. | 利用该反应可以除去Ti中的Si | |
| C. | 在100℃时,不可能有Ti存在 | |
| D. | 增加Ti固体的量有利于平衡向右移动 |
分析 A、气体的物质的量减少;
B、硅与碘不反应;
C、温度不同,反应方程式不同,产物不同;
D、Ti固体,固体的浓度是个常数.
解答 解:A、气体的物质的量减少,所以△S<0,故A错误;
B、硅与碘不反应,所以除去Ti中的Si,可以加碘蒸气,使其转化气体TiI4,故B正确;
C、在提纯过程中,高于200℃,碘和钛反应生成四氯化钛,所以在100℃时,有Ti存在,故C错误;
D、Ti固体,固体的浓度是个常数,所以增加Ti固体的量,平衡不移动,故D错误;
故选B.
点评 本题考查外界条件对化学平衡移动的影响,学生只要掌握平衡移动的原理就可以迅速解题,比较容易.

练习册系列答案
相关题目
15.取三张湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加98.3%的硫酸、新制氯水、浓氨水,三张试纸最后呈现的颜色是( )
| A. | 红、白、蓝 | B. | 黑、白、蓝 | C. | 白、白、蓝 | D. | 黑、红、蓝 |
16.有机物数量繁多的主要原因是( )
| A. | 有机物中含有多种元素 | B. | 碳原子最外层有4个电子 | ||
| C. | 有机物的副反应多 | D. | 有机物存在同分异构现象 |
13.下列离子方程式正确的是( )
| A. | 向盐酸中滴加氨水:H++OH-═H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O═2HClO+SO32- |
20.下列说法中不正确的是( )
| A. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| B. | 乙醇和乙酸都是常用调味品的主要成分,它们在一定条件下都可以发生取代反应 | |
| C. | 分子式为C4H9Cl的同分异构体共有4种(不考虑立体异构) | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
10.下列叙述正确的是( )
| A. | 同主族元素自上而下,得电子能力增强 | |
| B. | 最外层电子数小于4的一定是金属元素 | |
| C. | 同周期元素中ⅠA族元素的原子半径最小 | |
| D. | 酸性:HClO4>H2SO4>H3PO4 |
17.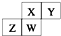 如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
 如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | z的最高正化合价与最低负化合价的绝对值可能相等 | |
| D. | w的最高价氧化物的水化物可能为弱酸,也有可能为强酸 |
14.下列大小比较正确的是( )
| A. | 酸性:HClO>H2SO4>H2CO3;非金属性Cl>S>C | |
| B. | 碱性:CsOH>KOH>Mg(OH)2>NaOH; 金属性:Cs>K>Mg>Na | |
| C. | 离子半径:Na+>Mg2+>Al3+>Cl-;原子半径:Na>Mg>Al>Cl | |
| D. | 稳定性:HF>H2O>NH3>CH4; 还原性:CH4>NH3>H2O>HF |