题目内容
15.如图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,正极的电极反应式为xS+2e-═Sx2-,M(由Na2O和Al2O3制得)的两个作用是导电和隔绝Na、S的作用.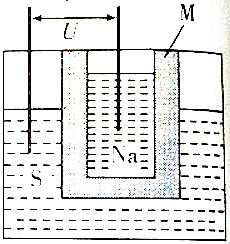
分析 由方程式可知反应中Na被氧化,应为原电池负极反应,电极方程式为Na-e?=Na+,S化合价降低,被还原,为原电池正极反应,电极方程式为xS+2e?→Sx2?,原电池工作时,M起到导电和隔绝Na、S的作用,以此解答该题.
解答 解:由方程式可知反应中Na被氧化,应为原电池负极反应,电极方程式为Na-e?=Na+,正极上硫得电子发生还原反应,所以正极电极反应式为:xS+2e-═Sx2-;原电池工作时,M起到导电和隔绝Na、S的作用,故答案为:xS+2e-═Sx2-;导电和隔绝Na、S的作用.
点评 本题考查了原电池原理,明确正负极上得失电子及反应类型是解本题关键,难点是电极反应式的书写,根据M晶体的类型确定M的导电作用,难度不大.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
5.在一定条件下,Ti和I2可以发生如下反应:Ti(s)+2I2(g)$→_{1300~1500℃}^{100~200℃}$ TiI4(g),下列说法正确的是( )
| A. | 该反应△S>0 | |
| B. | 利用该反应可以除去Ti中的Si | |
| C. | 在100℃时,不可能有Ti存在 | |
| D. | 增加Ti固体的量有利于平衡向右移动 |
6.L-多巴可用于治疗帕金森综合症,其结构简式为: ,下列关于它的叙述正确的是( )
,下列关于它的叙述正确的是( )
 ,下列关于它的叙述正确的是( )
,下列关于它的叙述正确的是( )| A. | L-多巴只含有2中官能团 | |
| B. | L-多巴不能发生肽反应 | |
| C. | L-多巴既具有酸性,又具有碱性 | |
| D. | 1molL-多巴只能与含1molNaOH的溶液反应 |
3.下列图象分别表示有关反应的反应过程与能量变化的关系据此判断下列说法中正确的是( )


| A. | 石墨转变为金刚石是吸热反应 | |
| B. | CO(g)+H2O(g)═CO2(g)+H2(g)是吸热反应 | |
| C. | 相同条件下,等质量S(g)和S(s)的能量比较,S(s)较大 | |
| D. | 白磷比红磷稳定 |
20.下列离子会发生水解反应而不能大量共存的是( )
| A. | Mg2+、OH-、NH4+、Na+ | |
| B. | c(H+)水=1.0×10-12mol•L-1的溶液中:S2-、Na+、OH-、K+ | |
| C. | S2-、Cl-、Al3+、SO42- | |
| D. | S2-、K+、Fe3+、Cl- |
7.以铬铁矿(主要成分是FeO•Cr2O3,含少量MgCO3、Al2O3、SiO2等)为原料制取铬酸钠(Na2CrO4)晶体的工艺流程如下:
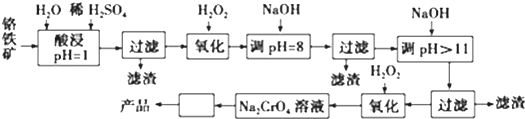
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下.
(1)流程中两次使用了H2O2,分别写出反应的离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O、2CrO2-+3H2O2+2OH-═2CrO42-+4H2O.
(2)流程图中“□”内的操作是蒸发浓缩、冷却结晶.
(3)加入NaOH调节溶液的pH=8时,被除去的离子是Fe3+、Al3+;调节溶液的pH>11时,被除去的离子是Mg2+.
(4)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么?不能,当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时Al(OH)3会溶解,引入杂质离子AlO2-.

已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下.
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8 | 9(>9溶解) |
(2)流程图中“□”内的操作是蒸发浓缩、冷却结晶.
(3)加入NaOH调节溶液的pH=8时,被除去的离子是Fe3+、Al3+;调节溶液的pH>11时,被除去的离子是Mg2+.
(4)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么?不能,当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时Al(OH)3会溶解,引入杂质离子AlO2-.
4.阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1molFeI2与足量氯气反应时转移的电子数为3NA | |
| B. | 1L2mol•L-1 K2S溶液中S2-和HS-的总数为2NA | |
| C. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| D. | 50mL18mol•L-1浓硫酸与足量铜微热反应,转移的电子数为1.8NA |