题目内容
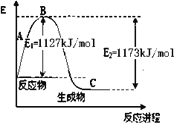
【题目】氨气是一种重要的化工原料,工业上用N2和H2合成NH3。现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化示意图如下图。则N-H键键能为
化学键 | H-H | N≡N |
键能(kJ/mol) | 436 | 946 |
A. 248kJ/molB. 391kJ/molC. 862kJ/molD. 431kJ/mol
【答案】B
【解析】
据△H=反应物的活化能-生成物的活化能求得△H,△H=反应物键能和-生成物键能和。
△H=反应物的活化能-生成物的活化能=1127kJ·mol-1-1173kJ·mol-1=-92kJ·mol-1,热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ·mol-1,△H=反应物键能和-生成物键能和=946kJ·mol-1+3×436kJ·mol-1-6×Q(N-H)=-92kJ·mol-1,解得Q(N-H)=391kJ·mol-1,B项正确;
答案选B。

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目