题目内容
【题目】在相同温度和压强下,对反应CO2(g)+H2(g) ![]() CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
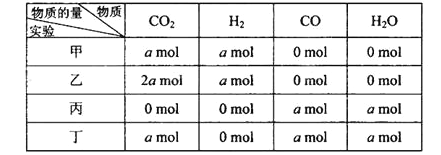
上述四种情况达到平衡后,n(CO)的大小顺序是( )
A. 乙=丁>丙=甲 B. 乙>丁>甲>丙
C. 丁>乙>丙=甲 D. 丁>丙>乙>甲
【答案】A
【解析】试题分析:该反应是一个气体体积不变的反应,等效平衡条件是采用“一边倒”方法转化后对应物质成比例即可。甲和乙均只有反应物,不需转化,对丙和丁进行“一边倒”转化,假设丙、丁中的CO、H2O(g)全部转化为CO2、H2,再与甲、乙比较:
CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
丙开始时 0mol 0mol amol amol
丙假设全转化 amol amol 0mol 0mol
丁开始时 amol 0mol amol amol
丁假设全转化 2amol amol 0mol 0mol
经转化后,甲、丙的起始浓度一样,乙、丁的起始浓度一样,且乙、丁的CO2的物质的量大于甲、丙的CO2的物质的量,相当于在甲或丙的基础上增加二氧化碳的浓度,使平衡正向移动,因此乙、丁平衡时的CO物质的量比甲、丙大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


