题目内容
下列物质的性质比较,不正确的是( )
| A、酸性:H2SO4>HClO4>HBrO4 |
| B、碱性:RbOH>KOH>NaOH |
| C、非金属性:Cl>S>P |
| D、气态氢化物稳定性:HF>HCl>HBr |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B.元素的金属性越强,对应的最高价氧化物的碱性越强;
C.同周期元素从左到右,元素的非金属性逐渐增强;
D.元素的非金属性越强,对应的氢化物越稳定.
B.元素的金属性越强,对应的最高价氧化物的碱性越强;
C.同周期元素从左到右,元素的非金属性逐渐增强;
D.元素的非金属性越强,对应的氢化物越稳定.
解答:
解:A.非金属性Cl>S,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故A错误;
B.金属性:Rb>K>Na,元素的金属性越强,对应的最高价氧化物的碱性越强,故B正确;
C.同周期元素从左到右,元素的非金属性逐渐增强,故C正确;
D.非金属性F>Cl>Br,元素的非金属性越强,对应的氢化物越稳定,故D正确.
故选A.
B.金属性:Rb>K>Na,元素的金属性越强,对应的最高价氧化物的碱性越强,故B正确;
C.同周期元素从左到右,元素的非金属性逐渐增强,故C正确;
D.非金属性F>Cl>Br,元素的非金属性越强,对应的氢化物越稳定,故D正确.
故选A.
点评:本题综合考查元素周期律知识,侧重于学生的分析能力的考查,为高频考点,注意把握比较的角度以及相关基础知识的积累,难度不大.

练习册系列答案
相关题目
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:
①过滤 ②蒸馏 ③静置分液 ④加入足量的金属钠 ⑤加入足量的NaOH溶液 ⑥通入过量的二氧化碳 ⑦加入足量的FeCl3溶液 ⑧加入乙酸与浓硫酸混合液加热.
合理的实验操作步骤及顺序是( )
①过滤 ②蒸馏 ③静置分液 ④加入足量的金属钠 ⑤加入足量的NaOH溶液 ⑥通入过量的二氧化碳 ⑦加入足量的FeCl3溶液 ⑧加入乙酸与浓硫酸混合液加热.
合理的实验操作步骤及顺序是( )
| A、④⑤③ | B、⑥①⑤③ |
| C、⑧①⑦③ | D、⑤②⑥③ |
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4,下列说法正确的是( )
| A、W、Y、Z的非金属性大小顺序一定是Z>Y>W |
| B、W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C、Y、Z形成的分子空间构型可能是正四面体 |
| D、XZ3中含有离子键 |
某无色溶液中能大量共存的一组离子是( )
| A、OH-、Ba2+、NH4+、Cl- |
| B、K+、Fe2+、H+、NO3- |
| C、NH4+、Al3+、Cl-、NO3- |
| D、Mg2+、SO42-、SiO32-、H+ |
下列说法不正确的是( )
| A、化学反应除了生成新物质外,还伴随着能量的变化 |
| B、物质燃烧和中和反应均放出热量 |
| C、分解反应肯定是吸热反应 |
| D、化学反应是吸热还是放热决定于生成物具有的总能量和反应物具有的总能量 |
下列说法正确的是( )
| A、32g O2占有的体积约为22.4L |
| B、22g二氧化碳与标准状况下11.2L HCl含有相同的分子数 |
| C、标准状况下,22.4L水的质量约为18g |
| D、22.4L N2含有阿伏加德罗常数个N2 |
下列说法正确的是( )
| A、键能越大,表示该分子越容易受热分解 |
| B、共价键都具有方向性 |
| C、在分子中,两个成键的原子间的距离叫键长 |
| D、H-Cl的键能为431.8kJ?mol-1,H-Br的键能为366kJ?mol-1,说明HCl比HBr分子稳定 |
下列说法不正确的是( )
| A、体系有序性越高,熵值就越低 |
| B、一杯热水变冷是焓减少的过程 |
| C、吸热反应不可以自发进行 |
| D、同种物质气态时熵值最大 |
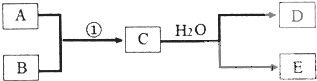 已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:
已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系: